256: SARSコロナウイルス2型のスパイクと抗体(SARS-CoV-2 Spike and Antibodies)
著者: David S. Goodsell
翻訳: 工藤 高裕(PDBj)
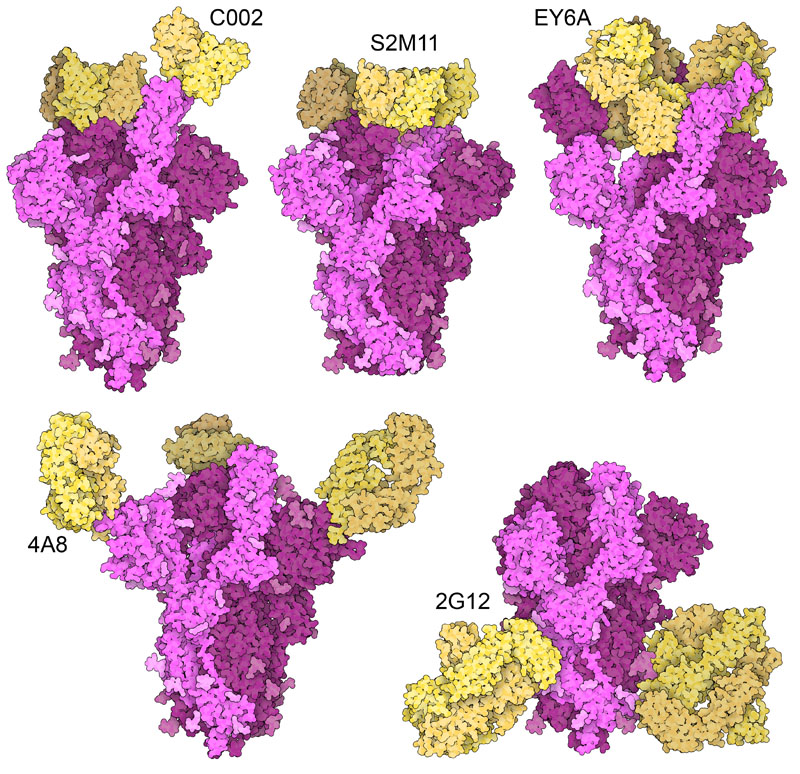
抗体Fab断片(黄)がSARS-CoV-2スパイクタンパク質(赤紫)に結合した構造。すべての構造は抗体の可変ドメインを含み、中には定常ドメインも伴っているものもある。
高解像度TIFF画像は
こちら。
構造生物学者たちはCOVID-19(SARSコロナウイルス2型感染症)大流行との戦いに力を注いできた。世界中の研究所では、ウイルスのほぼすべての側面において研究を行い、感染と戦う際に標的となり得る弱点を探している。スパイクタンパク質(spike protein)はこの取り組みの主たる注目対象となっている。なぜならこれがウイルスの生活環において不可欠な役割を果たし、私たちの免疫系が防御するときの主な標的になっているからである。このウイルスが出現してから1年程の間に、何百ものスパイクタンパク質の構造が決定され、その柔軟性や細胞受容体ACE2との相互作用、そして免疫が中和抗体(neutralizing antibody)を使ってウイルスをブロックする方法の詳細が明らかになった。
驚くべき抗体
ここにスパイクに抗体がついた構造をいくつか示す。抗体がタンパク質を認識する方法はたくさんあるが、ここではその中のいくつかを取り上げている。このうちの4つは、SARSコロナウイルス2型(SARS-CoV-2)に感染した患者から単離されたものである。上の3つはスパイクの受容体結合ドメイン(receptor-binding domain)を認識するが、それぞれ方法は違っている。抗体断片C002(PDBエントリー7k8t)はACE2を認識する部位に結合するが、それは活性のあるup型、活性のないdown型、どちらの状態の受容体結合ドメインに対しても行われる。S2M11(PDBエントリー7k43)はまた別の方法で結合し、受容体結合ドメインを下の位置に固定する。EY6A(PDBエントリー6zdh)の場合はドメインのさらに下の位置に結合する。下に示す2つの抗体は、全く違ったやり方で結合している。4A8(PDBエントリー7c2l)が結合するのは隣接したドメインだが、それでもスパイクを働かなくする。2G12(PDBエントリー7l06)はHIV-1感染によってできた珍しい抗体で、SARSコロナウイルス2型にも結合はするが働きは無効化されない。これにはドメインが入れ替わった抗体が2つ含まれ、ともにスパイク表面にある糖を認識する。
組み合わせ攻撃
もちろん、この研究の主な目的は、人々を感染から守り、感染した患者の治療方法を開発することである。この研究を大きく推し進めた重要な知見の一つは、抗体がスパイクを認識する方法はさまざまなものがあるということであった。この知見は、複数種の抗体の混合して使う組み合わせ治療や、さまざまな種類の抗体を引き出すよう設計された組み合わせワクチンの開発につながる糸口となっている。さまざまな方法でスパイクを標的とする組み合わせ手法が、抵抗株の出現を制御することに役立つかもしれない。HIV-1の治療でも見られたように、複数種の薬が同時に攻めてくるのを避けつつ変異しなければならないなら、ウイルスは抵抗性を獲得するのがずっと難しくなる。
ナノ抗体
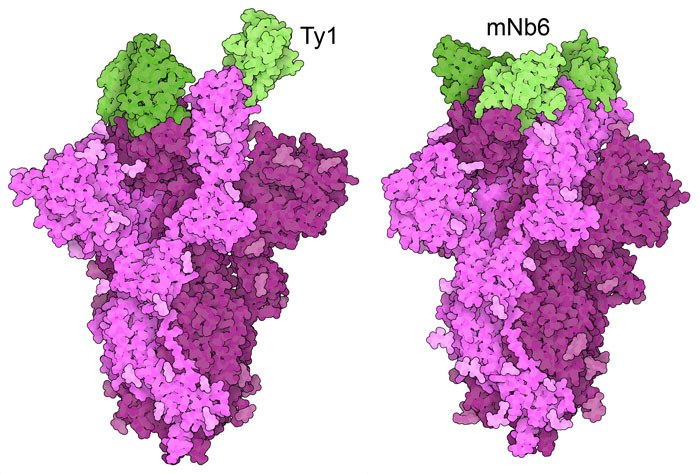
ナノボディ(緑)がSARSコロナウイルス2型のスパイクタンパク質(赤紫)に結合した構造。
高解像度TIFF画像は
こちら。
ナノボディ(nanobody)と呼ばれる、より小さなサイズで設計された抗体の中で病気の治療に使えるものがないかを探す試みも行われている。ここにそのような事例を2つ示す。1本鎖の抗体Ty1(PDBエントリー6zxn)はウイルスのスパイクをアルパカに接種し免疫をつくらせることにより見つかった。これは受容体結合ドメインに結合するが、開いたup状態でも閉じたdown状態でも結合することができ、ACE2受容体への結合を妨げる。ナノボディのmNb6(PDBエントリー7kkl)は、合成ナノボディのライブラリから選び出し、その後スパイクと相互作用する部分に多くの微修正を加え、最も強く結合するものを選りすぐって最適化されたものである。これは不活性なdown配置にある受容体結合ドメインに結合する。
構造をみる
対話的操作のできるページに切り替えるには図の下のボタンをクリックしてください。読み込みが始まらない時は図をクリックしてみてください。
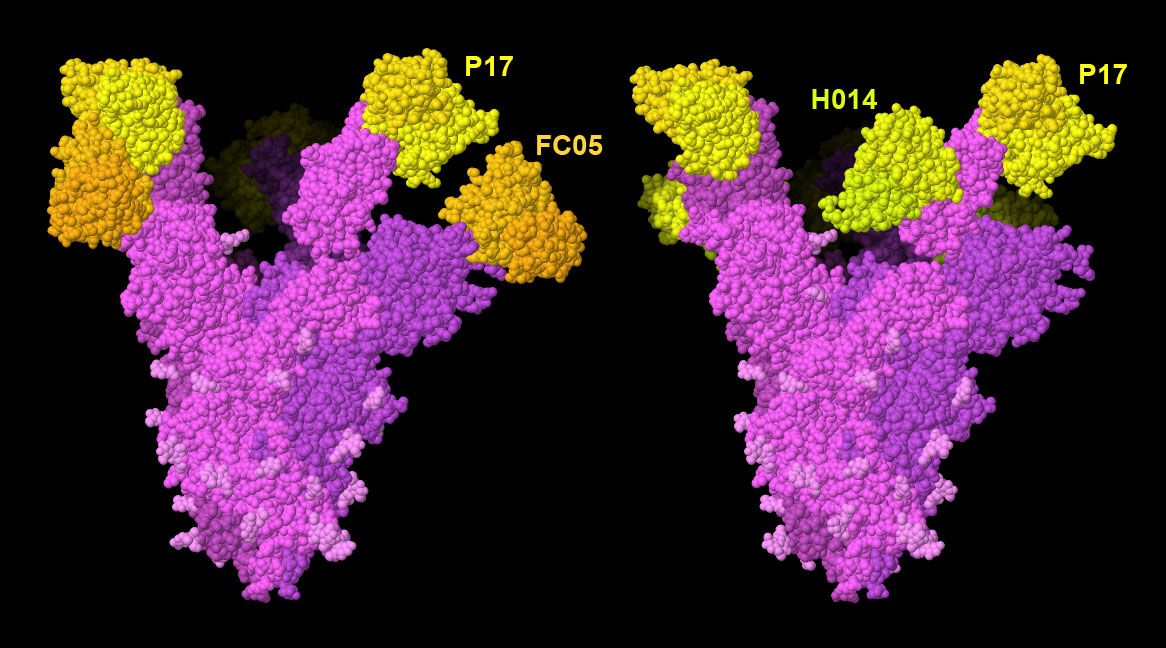
構造生物学者は今、どうすれば混ぜ合わせた複数種の抗体を一緒に働かせ、ウイルスの機能を止めることができるのかを調べている。ここに2つの事例を示す。左に示すのはPDBエントリー7cwuの構造で、P17が受容体結合ドメインを阻害し、FC05がドメインのN末端に結合している。右に示すのはPDBエントリー7cwnの構造で、受容体結合ドメインの下側部位に結合しているH014がP17と組み合わさっている。画像の下のボタンをクリックして対話的操作のできる画像に切り替え、これらの構造をより詳しく見てみて欲しい。
理解を深めるためのトピックス
-
抗体やスパイクそのものの構造だけではなく、スパイクやスパイクドメインに結合した抗体の構造も多数PDBで見ることができる。
-
これらの構造を見るとき、多少の想像力を必要とする。最初の図の説明で述べたように、ここに示すいずれの構造も抗体の可変ドメイン(variable domain)は含んでいるが、定常ドメイン(constant domain)部分の座標については一部の構造にしか含まれていない。さらに、スパイクの膜貫通部分は見えていなくて、通常、多くの糖鎖修飾部位に最初数単位の糖だけが含まれている。
参考文献
-
7k8t
Barnes, C.O., Jette, C.A., Abernathy, M.E., Dam, K.A., Esswein, S.R., Gristick, H.B., Malyutin, A.G., Sharaf, N.G., Huey-Tubman, K.E., Lee, Y.E., Robbiani, D.F., Nussenzweig, M.C., West Jr., A.P., Bjorkman, P.J. (2020) SARS-CoV-2 neutralizing antibody structures inform therapeutic strategies. Nature 588: 682-687
-
7c2l
Chi, X., Yan, R., Zhang, J., Zhang, G., Zhang, Y., Hao, M., Zhang, Z., Fan, P., Dong, Y., Yang, Y., Chen, Z., Guo, Y., Zhang, J., Li, Y., Song, X., Chen, Y., Xia, L., Fu, L., Hou, L., Xu, J., Yu, C., Li, J., Zhou, Q., Chen, W.
2020
A neutralizing human antibody binds to the N-terminal domain of the Spike protein of SARS-CoV-2.
Science
369
650-655
-
6zxn
Hanke, L., Vidakovics Perez, L., Sheward, D.J., Das, H., Schulte, T., Moliner-Morro, A., Corcoran, M., Achour, A., Karlsson Hedestam, G.B., Hallberg, B.M., Murrell, B., McInerney, G.M.
2020
An alpaca nanobody neutralizes SARS-CoV-2 by blocking receptor interaction.
Nat Commun
11
4420-4420
-
7kkl
Schoof, M., Faust, B., Saunders, R.A., Sangwan, S., Rezelj, V., Hoppe, N., Boone, M., Billesbolle, C.B., Puchades, C., Azumaya, C.M., Kratochvil, H.T., Zimanyi, M., Deshpande, I., Liang, J., Dickinson, S., Nguyen, H.C., Chio, C.M., Merz, G.E., Thompson, M.C., Diwanji, D., Schaefer, K., Anand, A.A., Dobzinski, N., Zha, B.S., Simoneau, C.R., Leon, K., White, K.M., Chio, U.S., Gupta, M., Jin, M., Li, F., Liu, Y., Zhang, K., Bulkley, D., Sun, M., Smith, A.M., Rizo, A.N., Moss, F., Brilot, A.F., Pourmal, S., Trenker, R., Pospiech, T., Gupta, S., Barsi-Rhyne, B., Belyy, V., Barile-Hill, A.W., Nock, S., Liu, Y., Krogan, N.J., Ralston, C.Y., Swaney, D.L., Garcia-Sastre, A., Ott, M., Vignuzzi, M., Walter, P., Manglik, A.
2020
An ultrapotent synthetic nanobody neutralizes SARS-CoV-2 by stabilizing inactive Spike.
Science
370
1473-1479
-
7k43
Tortorici, M.A., Beltramello, M., Lempp, F.A., Pinto, D., Dang, H.V., Rosen, L.E., McCallum, M., Bowen, J., Minola, A., Jaconi, S., Zatta, F., De Marco, A., Guarino, B., Bianchi, S., Lauron, E.J., Tucker, H., Zhou, J., Peter, A., Havenar-Daughton, C., Wojcechowskyj, J.A., Case, J.B., Chen, R.E., Kaiser, H., Montiel-Ruiz, M., Meury, M., Czudnochowski, N., Spreafico, R., Dillen, J., Ng, C., Sprugasci, N., Culap, K., Benigni, F., Abdelnabi, R., Foo, S.C., Schmid, M.A., Cameroni, E., Riva, A., Gabrieli, A., Galli, M., Pizzuto, M.S., Neyts, J., Diamond, M.S., Virgin, H.W., Snell, G., Corti, D., Fink, K., Veesler, D.
2020
Ultrapotent human antibodies protect against SARS-CoV-2 challenge via multiple mechanisms.
Science
370
950-957
-
6zdh
Zhou, D., Duyvesteyn, H.M.E., Chen, C.P., Huang, C.G., Chen, T.H., Shih, S.R., Lin, Y.C., Cheng, C.Y., Cheng, S.H., Huang, Y.C., Lin, T.Y., Ma, C., Huo, J., Carrique, L., Malinauskas, T., Ruza, R.R., Shah, P.N.M., Tan, T.K., Rijal, P., Donat, R.F., Godwin, K., Buttigieg, K.R., Tree, J.A., Radecke, J., Paterson, N.G., Supasa, P., Mongkolsapaya, J., Screaton, G.R., Carroll, M.W., Gilbert-Jaramillo, J., Knight, M.L., James, W., Owens, R.J., Naismith, J.H., Townsend, A.R., Fry, E.E., Zhao, Y., Ren, J., Stuart, D.I., Huang, K.A.
2020
Structural basis for the neutralization of SARS-CoV-2 by an antibody from a convalescent patient.
Nat Struct Mol Biol
27
950-958
-
7cws
Wang, N., Sun, Y., Feng, R., Wang, Y., Guo, Y., Zhang, L., Deng, Y.Q., Wang, L., Cui, Z., Cao, L., Zhang, Y.J., Li, W., Zhu, F.C., Qin, C.F., Wang, X.
2021
Structure-based development of human antibody cocktails against SARS-CoV-2.
Cell Res
31
101-103
-
7cwn
Yao, H., Sun, Y., Deng, Y.Q., Wang, N., Tan, Y., Zhang, N.N., Li, X.F., Kong, C., Xu, Y.P., Chen, Q., Cao, T.S., Zhao, H., Yan, X., Cao, L., Lv, Z., Zhu, D., Feng, R., Wu, N., Zhang, W., Hu, Y., Chen, K., Zhang, R.R., Lv, Q., Sun, S., Zhou, Y., Yan, R., Yang, G., Sun, X., Liu, C., Lu, X., Cheng, L., Qiu, H., Huang, X.Y., Weng, T., Shi, D., Jiang, W., Shao, J., Wang, L., Zhang, J., Jiang, T., Lang, G., Qin, C.F., Li, L., Wang, X.
2021
Rational development of a human antibody cocktail that deploys multiple functions to confer Pan-SARS-CoVs protection.
Cell Res
31
25-36
-
7l06
Acharya, P., Williams, W., Henderson, R., Janowska, K., Manne, K., Parks, R., Deyton, M., Sprenz, J., Stalls, V., Kopp, M., Mansouri, K., Edwards, R.J., Meyerhoff, R.R., Oguin, T., Sempowski, G., Saunders, K., Haynes, B.F.
2020
Biorxiv
DOI:10.1101/2020.06.30.178897


 の生体高分子学習ポータルサイト
の生体高分子学習ポータルサイト 









