142: PDBの先駆者たち(PDB Pioneers)
構造生物学(Structural biology)は1958年、ジョン・ケンドリュー(John Kendrew)によるミオグロビン(myoglobin)の原子構造によって誕生し、その後数十年で急速に発展した。1970年代初頭、分かっていたタンパク質の構造は12種類だけだったが、この中に素晴らしい情報が詰まっていることが発見された。ところが、これらの構造を収めた座標ファイルは極めて大きく、インターネットがまだなかった当時、個々の研究者が世界中で増えつつあるその構造に関心を持った構造生物学者とこれらの巨大なファイルを共有するのは容易ではなかった。この問題を解決するため、データのアーカイブ(保管庫)となる「タンパク質構造データバンク」(Protein Data Bank、PDB)が創設された。登録者は原子座標データをPDBに送り、その後関心を持ったユーザにも送っていた。では、PDB創立40周年を記念して、PDBアーカイブ設立に影響を与えた歴史的タンパク質の構造をみていくことにしよう。
酸素の輸送
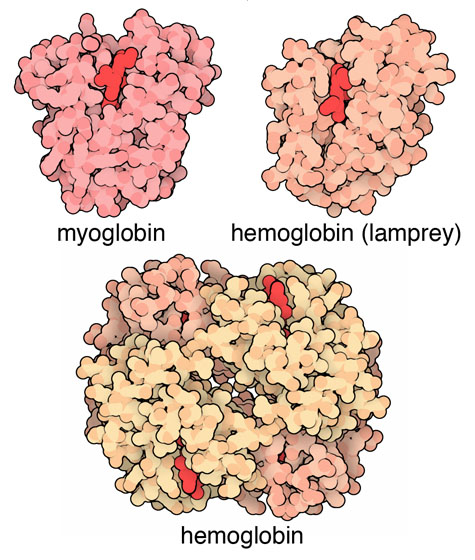
ジョン・ケンドリューによるミオグロビン(PDBエントリー 1mbn)の構造では、どのようにしてタンパク質鎖が補欠分子族やリガンドと相互作用し、タンパク質鎖がどのようにして折りたたまれるのかについて、初めて明らかとなった。また、マックス・ペルーツ(Max Perutz)によるヘモグロビン(hemoglobin、PDBエントリー 2dhb)の構造によってこの話は更に発展し、どのようにして似た4本の鎖が集合でき、少しの形状変化でリガンドの結合を制御できるのかが示された。初期のPDBにはもう一つこのファミリーに属するタンパク質が含まれていた。それがヤツメウナギ(lamprey)由来のヘモグロビン(PDBエントリー 2lhb)で、ミオグロビンと私たちのヘモグロビンとの中間に当たる分子である。これは単量体と二量体の間を行き来することで活性を制御している。
酵素の活性部位
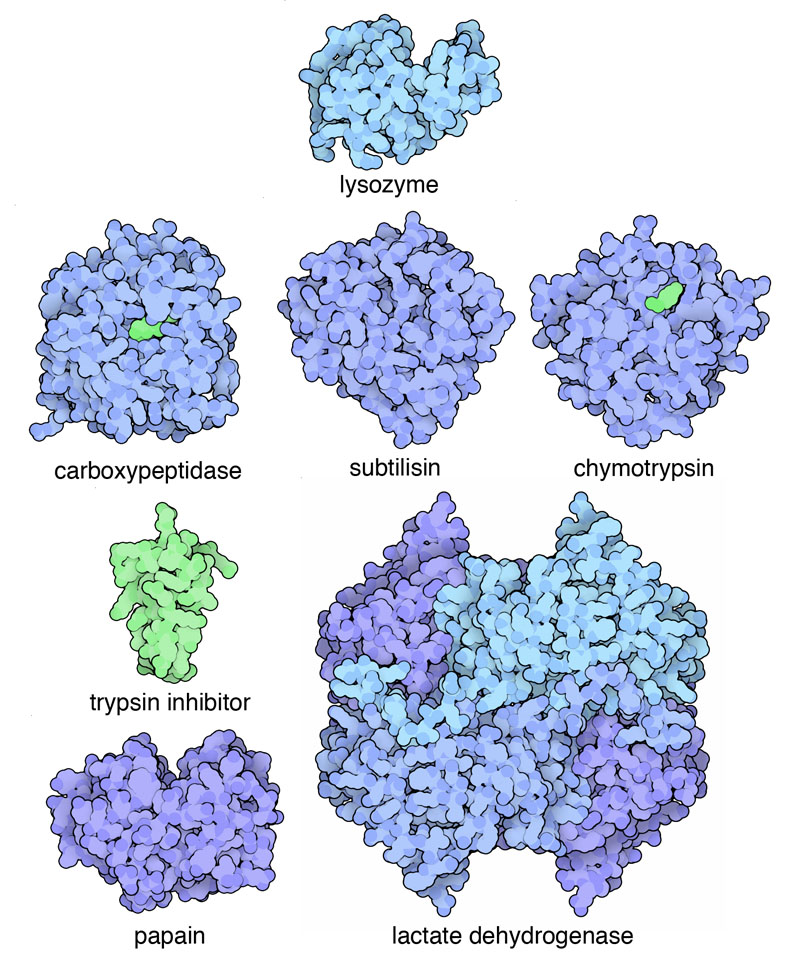
初期のPDBには酵素もいくつか登録されていたが、これによりタンパク質鎖がどのようにして化学的触媒となるよう折りたたまれるのかが明らかになった。DC・フィリップスによるリゾチーム(lysozyme、PDBエントリー 1lyz)は1965年に解かれ1975年にPDBへ登録された構造で、これから酵素は基質の形に合う活性部位を持っていることが明らかになった。更に彼らは、注意深く分子設計を行う手法を用いて、リゾチームは基質を変形させることで基質を切断しやすくしているという仕組みを提案した。当時の記憶媒体であるPDBの磁気テープには、カルボキシペプチダーゼ(carboxypeptidase、3cpa)、スブチリシン(subtilisin、1sbt)、キモトリプシン(chymotrypsin、2cha)、パパイン(papain、9pap)といったタンパク質切断酵素に加え、小さな阻害剤タンパク質である膵臓トリプシン阻害剤(pancreatic trypsin inhibitor、4pti)も収められていた。また初期のPDBにおいて最も大きな構造は、4個のサブユニットが集まってできた乳酸脱水素酵素(lactate dehydrogenase、6ldh)で、各サブユニットに334個のアミノ酸を含む当時としては画期的なものであった。
電子の輸送
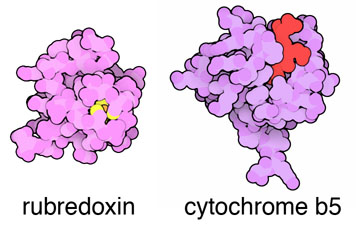
初期のPDBに登録されていた2つの構造、ルブレドキシン(rubredoxin、4rxn)とシトクロムb5(cytochrome b5、1cyo)では、タンパク質がどのようにして最も小さい荷物である個々の電子を運ぶのかが明らかになった。どちらのタンパク質も電子を輸送するのに鉄原子(iron atom)を使うが、その輸送方法は両者で異なっている。ルブレドキシンは鉄イオン(iron ion)を4つの硫黄原子(sulfur atom)でできた籠の中に捕らえている。この硫黄原子はタンパク質鎖のシステイン(cysteine)アミノ酸から提供されているものである。一方、シトクロムb5はヘム基(heme group)を使って鉄原子を然るべき場所に配置している。
構造をみる
対話的操作のできるページに切り替えるには図の下のボタンをクリックしてください。読み込みが始まらない時は図をクリックしてみてください。
このような先駆けとなる構造のPDBファイルはこの40年の間に修正され、改善されてきたものが多いが、その全てを今でもPDBのデータベースで参照することができる。もちろん、今日ではメールでデータが届くのを待つ必要はなく、ただインターネット経由でダウンロードしさえすればよい。あるいはここで示す対話的操作のできる画像でどの構造を表示するのか切り替えて参照してもよい。これらを参照する際、これらのタンパク質は小さく折りたたまれており、豊富に存在するタンパク質であることに注目して欲しい。この特徴があるからこそ初期の構造は解くことができたのである。なぜなら初期のタンパク質結晶化技術では大量の精製されたタンパク質と、大量の安定な結晶が必要であったからである。今日では、より洗練された結晶化技術と非常に強力なシンクロトロンX線源を使うことで、より大きくより複雑な分子を、より少量の試料で構造を解けるようになっている。
理解を深めるためのトピックス
ここで紹介した初期の構造は各タンパク質に関する最初の視点を与えてくれますが、これはある状態をとらえたスナップショットの一つに過ぎません。いずれの場合も、後になって解かれた構造によってタンパク質が働く仕組みを説明する生物学的ストーリーが明らかになっています。PDBには変異の効果、リガンドや阻害剤の結合、タンパク質の動き、そして機能を他の視点から見たものを示す別の構造も登録されています。例えば、次に示すような構造を見ることができるでしょう。
- ヘモグロビンのアロステリックな動き(活性制御分子の結合・解離によるタンパク質の構造変化)
- ヘモグロビンの生物間での違い
- 膵臓トリプシン阻害剤がトリプシンへどのように結合するのか
- リゾチームにおける変異の影響
- 補因子NADHがどのように乳酸脱水素酵素へ結合するのか
参考文献
- 1958 A three-dimensional model of the myoglobin molecule obtained by x-ray analysis. Nature 181 662-666
- 1965 Structure of hen egg-white lysozyme, a three-dimensional Fourier synthesis at 2 Angstroms resolution. Nature 206 757-761
- 1970 Three dimensional Fourier synthesis of horse deoxyhaemoglobin at 2.8 Angstrom units resolution. Nature 228 551-552
- 1977 The Protein Data Bank: a computer-based archival format for macromolecular structures. Journal of Molecular Biology 112 535-542
- 2008 The Protein Data Bank: a historical perspective. Acta Crystallographica Section A 64 88-95
代表的な構造
- 1mbn: マッコウクジラのミオグロビン
- ミオグロビンは酸素を細胞内に蓄えるタンパク質で、特に筋肉細胞で豊富に見られる。この歴史的構造は初めて構造が明らかになったタンパク質で、ジョン・ケンドリューの研究所で解かれたものである。
- 2dhb: ウマのデオキシヘモグロビン
- ヘモグロビンは血液中で酸素を輸送するタンパク質である。この歴史的構造は複数のサブユニットで構成されるタンパク質としては初めて構造が明らかになったタンパク質で、マックス・ペルーツの研究所で解かれたものである。
- 2lyz: リゾチーム
- リゾチームは細菌の細胞壁にある糖鎖を切断する小さな酵素で、私たちの身体を感染から保護するのに使われる。この歴史的構造は初めて構造が明らかになった酵素で、D.C.フィリップスの研究所で解かれたものである。
 の生体高分子学習ポータルサイト
の生体高分子学習ポータルサイト 









