289: メディエータ(Mediator)
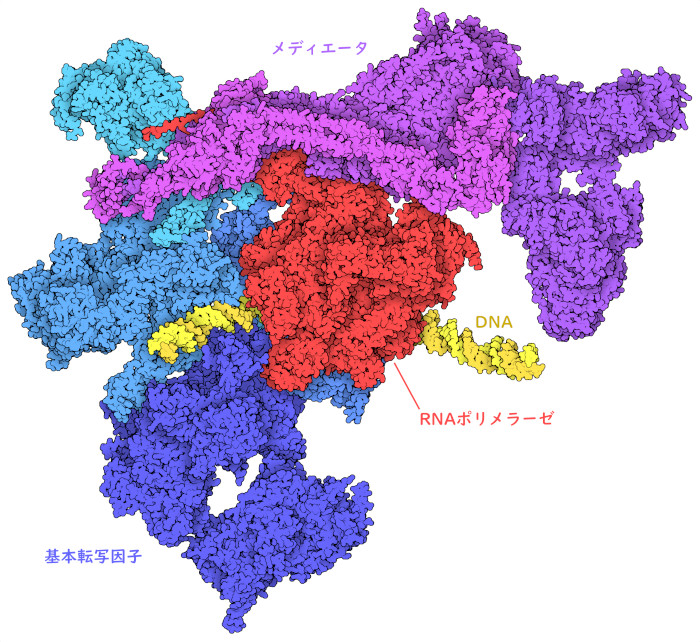
驚くべきことに、私たちの細胞は、私たちが生涯を通じて行うすべての仕事を管理するのに、たった2万種程度のタンパク質しか必要としない。もちろん、これらのタンパク質をいつどこで作り使うのかを制御することが重要である。例えば、筋肉細胞にはたくさんのミオシン(myosin)があり、神経細胞にはイオンチャネル、輸送体、受容体が適切に組み合わされている。こうした選択のほとんどは、転写(transcription)のレベルで行われる。細胞は、伝令RNA(messenger RNA)分子をどのタイミングで作り(転写を行い)、タンパク質の合成に使えるようにするのかを注意深く制御している。なお、この伝令RNAはRNAポリメラーゼII(RNA polymerase II)によって特定の遺伝子から作られている。DNAの側鎖へ特異的に結合する制御タンパク質である転写因子(transcription factor)は1600種類以上あり、これらが協力して転写のタイミングを決め、細胞の現状を監視し、行動が必要かどうかを決定している。約30種類のタンパク質鎖で構成される大きなタンパク質複合体メディエータ(mediator)は、これら多くの入力を統合し、体内において特定のタンパク質が必要とされる場所と時間に合わせてRNAポリメラーゼIIを動員する。
はじめに
ここに示すのは、PDBエントリー7encで登録されている、転写を開始する準備を整えた「転写開始前複合体」(pre-initiation complex)の構造である。この複合体には、真核生物のメディエータとRNAポリメラーゼII、ゲノムにコードされた情報に基づいて伝令RNAをつくる主要なRNAポリメラーゼが含まれる。また、転写開始前複合体には、基本転写因子(general transcription factor、後述)の集合体も含まれている。この転写因子は、遺伝子の転写開始部位を認識し、DNA二重らせんの2本の鎖を分離して、RNAポリメラーゼによる転写開始を促進するという必要な仕事を行う。ところが、現在わかっているメディエータの構造から、この複合体の重要な機能に関する情報を得ることはできない。また、どの遺伝子を転写する必要があるのかを決めているその他何百もの転写因子とも相互作用している。これら相互作用の構造的な詳細は、まだほとんど謎のままである。
距離を隔てた相互作用
私たちが持つ転写因子のほとんどは、プロモーターの近くや遠位エンハンサーエレメント(distal enhancer element)のように開始部位とは別の場所にあるDNA中の制御領域に結合する。メディエータはこれらの転写因子と相互作用し、いつ転写開始前複合体を構築する必要があるかを決める手助けをする。そして、これらの相互作用について多くの興味深い側面が明らかにされてきた。メディエータを構成するサブユニットのいくつかは相互作用に重要で、特に図の右側に示すフォーク形の尾部にあるサブユニットが重要である。メディエータは、目的のゲノムとは離れた制御部位で転写因子と相互作用し、遠位エンハンサーと転写開始前複合体との橋渡しをすることができる。さらに問題を複雑にしているのは、これらの相互作用のいくつかは、メディエータサブユニットまたは転写因子の本質的に構造が定まっていない領域に関わっている可能性があり、おそらくメディエータと制御タンパク質を一緒にする相分離した液滴を形成していることが明らかになりつつあることである。
基本転写因子
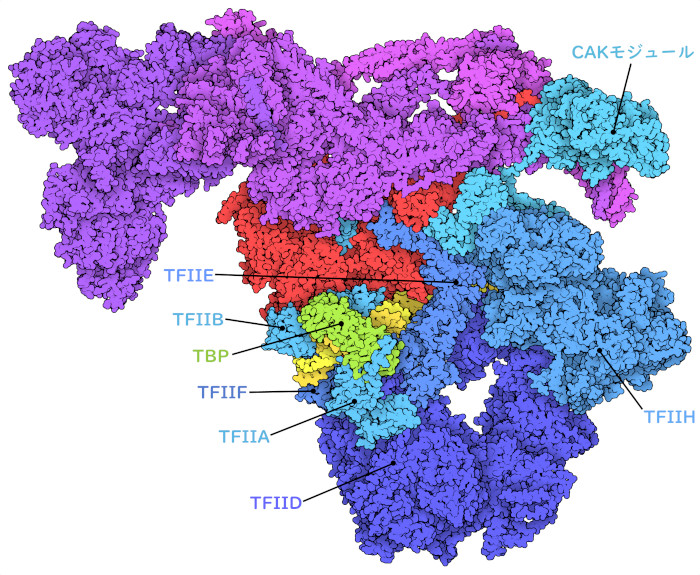
この構造は、転写開始前複合体においてRNAポリメラーゼを受け止めている基本転写因子の配置を明らかにしている。TATA結合タンパク質(TATA-binding protein、TFIIDの一部であるTBP)は過程を開始させる中心的な役割を果たしていて、AT(アデニンとチミン)が多い特徴的な配列に結合しDNAを鋭く曲げる分子サドルとして機能する。TFIIAとTFIIBはDNA周辺の領域と相互作用し、TFIIFとともに転写開始点におけるRNAポリメラーゼIIの位置決めを助ける。TFIIE、TFIIH、および他のTFIIDサブユニットは、複合体にさらなる機能性をもたらす。特に、TFIIHの一部は、転写に備えてDNA2本鎖を分離する転位酵素(translocase)であり、TFIIHのCAKモジュールは、RNAポリメラーゼIIの長い尾部にリン酸基を付加し、mRNA合成を開始する時期が来たという信号を送る。
揺れ動く尾部
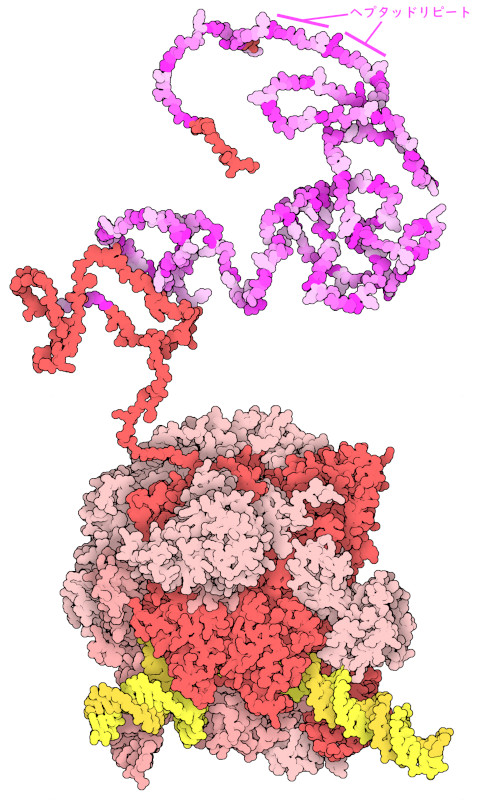
RNAポリメラーゼIIにおける最大のサブユニットはRPB1と呼ばれ、折りたたまれた構造をとらない長い尾を持っている(ここに示すのはPDBエントリー5iydと計算による構造モデルAF-AFP24928F1を組み合わせたもの)。このタンパク質は、セリンに富んだ特徴的なタンパク質配列(ヘプタッドリピート heptad repeatと呼ばれる7アミノ酸繰り返し配列)を52回繰り返している。それぞれの繰り返しにおいて、5番目のセリンはTFIIHのCAKモジュールによってリン酸化される。尾部が高度にリン酸化されると、メディエータとRNAポリメラーゼIIとの相互作用が弱まり、RNAポリメラーゼIIがmRNA合成を進めることができるようになる。また、リン酸化された鎖は、mRNAの前端を分解から守る珍しい化学的な覆いをつくる酵素を呼び寄せる。
構造をみる

対話的操作のできるページに切り替えるには図の下のボタンをクリックしてください。読み込みが始まらない時は図をクリックしてみてください。
メディエータは、制御信号を統合するという役割を担うにあたり、多くの異なるタンパク質と相互作用しなければならない。柔軟性を持つことでこれを実現し、さまざまな相手の構造的ニーズに対応している。3つの異なる構造を比較することで、この柔軟性の一端を見ることができる。ここに示すのは、メディエータ単独の構造を含むPDBエントリー6w1sと7enj、そしてPDBエントリー7lbmの転写開始前複合体である。さらに、これらの構造を調べてみると、メディエータタンパク質の多くの部分が構造には含まれていないことがわかる。これらの部分は本質的に定まった構造を取っておらず、自由に手を伸ばして周囲に来る相手と相互作用することができると考えられている。図の下にあるボタンをクリックして対話的操作のできる画像に切り替え、これらの構造をより詳しく見てみて欲しい。
理解を深めるためのトピックス
参考文献
- 2023 Regulation of RNA polymerase II pre-initiation complex by its associated coactivators. Nat Rev Genetics 24 767-782
- 2022 The Mediator complex as a master regulator of transcription by RNA polymerase II. Nat Rev Mol Cell Biol 23 732-749
- 7lbm 2021 Structure of the human Mediator-bound transcription preinitiation complex. Science 372 52-56
- 7enc, 7enj 2021 Structures of the human Mediator and Mediator-bound preinitiation complex. Science 372 eabg0635
- 6w1s 2019 A pliable Mediator acts as a functional rather than an architectural bridge between promoters and enhancers. Cell 178 1145-1158.e20
- 2018 The human transcription factors. Cell 172 650-665
- 5iyd 2016 Near-atomic resolution visualization of human transcription promoter opening. Nature 533 359-365
 の生体高分子学習ポータルサイト
の生体高分子学習ポータルサイト 









