288: 維生素(Vitamins)
健康的飲食必須包含細胞正常生長所需的所有營養素。這些營養物質包括蛋白質(protein)、核酸(nucleic acid)、碳水化合物(carbohydrate)和脂肪(fat),所有這些營養成分都會被分解並用於構建我們自己的分子並提供我們生存所需的能量。同時,我們也需要許多礦物質,例如血液中的血紅蛋白(hemoglobin)需要鐵,骨骼需要鈣。我們還需要少量的13種必要維生素。維生素是一種稀有的小分子,用於在我們的細胞中執行重要的工作。這些分子是健康生活所必需的,但我們的細胞無法製造它們。因此,我們需要從食物或維生素補充劑中獲取它們。
維生素的演變
這就提出了一個問題:如果這些分子如此重要,為什麼我們不能製造它們?和大多數與生物學相關的事物一樣,答案可以在演化中找到。在我們遠古祖先的演化過程中,這些分子可以在普通飲食中自由地攝取,因此沒有從頭開始製造它們的巨大壓力。另外,由於這些分子許多在化學層面上難以構建,因此存在著反對花費資源來製造它們的選擇性壓力。換句話說,在我們遙遠的家譜中的某個節點,製造這類分子帶來的安全性不足以支付相應的成本,因此便永遠失去了製造它們的能力。
自殺酶
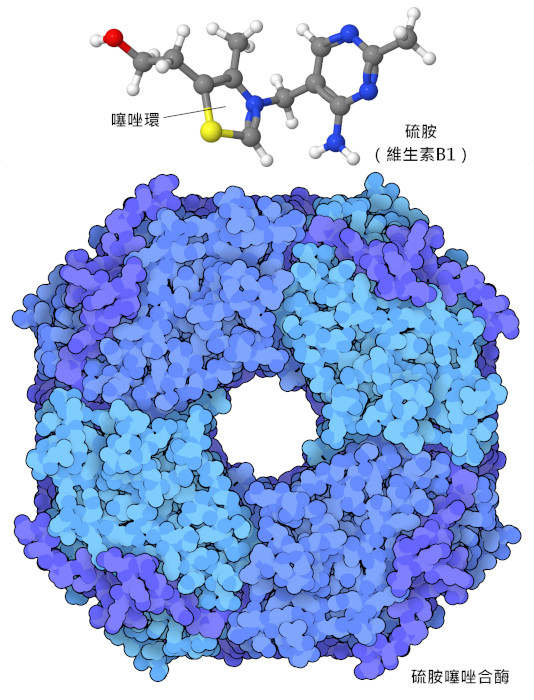
生成維生素B1(硫胺素)(vitamin B1 (thiamine))的酵素就是這種演化權衡的一個很好的例子。在植物和酵母細胞中,不同尋常的噻唑環(thiazole ring)是由硫胺噻唑合成酶(thiamine thiazole synthase)產生的。當研究人員研究了這種酵素的結構(PDB ID 3fpz)時,他們發現鏈中位於205 位的一個半胱氨酸缺失了一個硫原子。進一步的研究表明,該酵素在反應過程中提供了這個硫原子,並用它來建構噻唑環。因此,硫胺-噻唑合成酶是一種"自殺酶",只能起一次作用。這使得硫胺素的生產成本非常高,而酵母細胞必須大量生產這種蛋白質。由於我們(和其他動物)食用富含硫胺素的植物,因此我們不必承擔製造這種一次性酵素的成本,也不必自己製造硫胺素。
致命後果
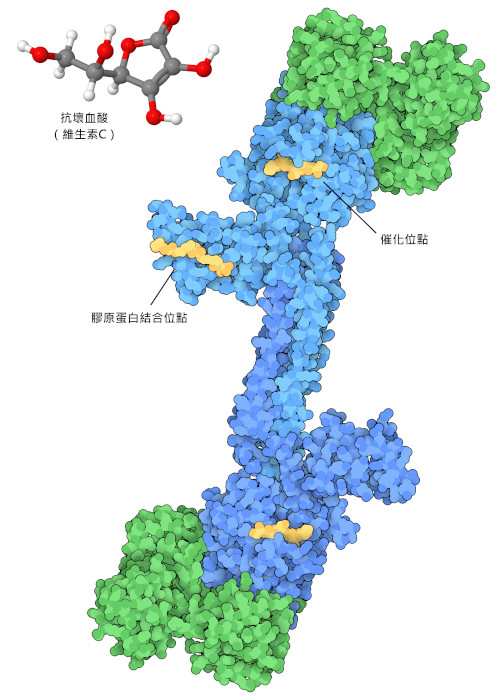
維生素是透過其與歷史疾病的關聯而被發現的,這些疾病是由於人們沒有這種分子的飲食來源而引起的。例如,幾個世紀前,遠航的水手患有壞血病(scurvy),這是一種因無法製造膠原蛋白( collagen)而引起的疾病。原因是飲食中缺乏維生素C(抗壞血酸)(vitamin C (ascorbic acid)),最終透過在航行中攜帶大量柑橘類水果解決了這個問題。今天,我們可以在分子層面上詳細了解這種疾病的細節。膠原脯氨酰4-羥化酶(collagen prolyl 4-hydroxylase,此處顯示的是PDB 條目7zsc和4bta的結構)將脯氨酸(proline)轉化為羥基脯氨酸(hydroxyproline),這對於健康結締組織中膠原纖維的緊密堆積和相互作用至關重要。該酵素在此反應中使用鐵硫簇,且不必要的副反應有時會使該簇失去活性。這就是維生素C發揮作用的地方:它是一種強大的抗氧化劑,可以恢復鐵原子的適當氧化狀態,從而恢復酶的活性。
吃紅蘿蔔
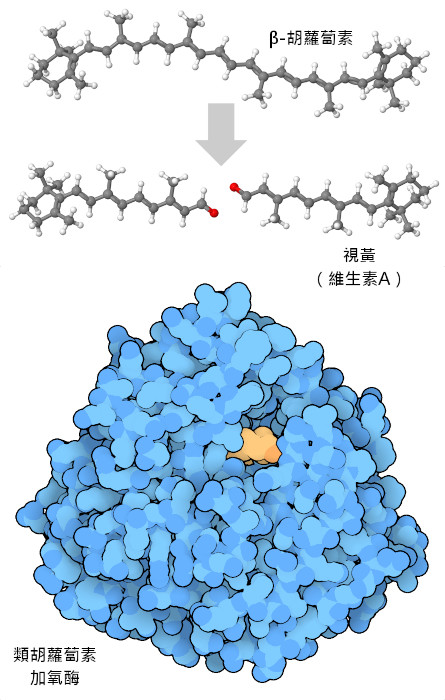
我們從食物中獲得大部分維生素,但在現代社會,許多加工食品都添加了維生素,確保我們隨時都能攝取足夠的維生素。在大多數情況下,我們直接從食物中獲取維生素。這是因為我們食用的植物和動物在它們自己的細胞中使用維生素的方式與我們相同。在其他情況下,維生素是從用於其他功能的分子中產生的。例如,植物中含有色彩豐富的β-胡蘿蔔素(beta-carotene)分子,它能吸收特定波長的光,從而呈現出鮮豔的顏色。胡蘿蔔是β-胡蘿蔔素的典型來源,這種成分使胡蘿蔔呈現橙色。我們的細胞利用胡蘿蔔素加氧酶(carotene oxygenase)將β-胡蘿蔔素分成兩個獨立的分子,每個分子都是一個有效的維生素A(視黃醛)(vitamin A (retinal))分子。視黃醛也會吸收光線,在我們的眼中是由受體蛋白視紫紅質(rhodopsin)來使用它的。這裡顯示的是一種源自藍藻的蛋白質(PDB 條目2biw),與製造視黃醛的酵素相似。也可以在AF_AFQ9HAY6F1中找到預測人類酵素的模型。
交易的藝術
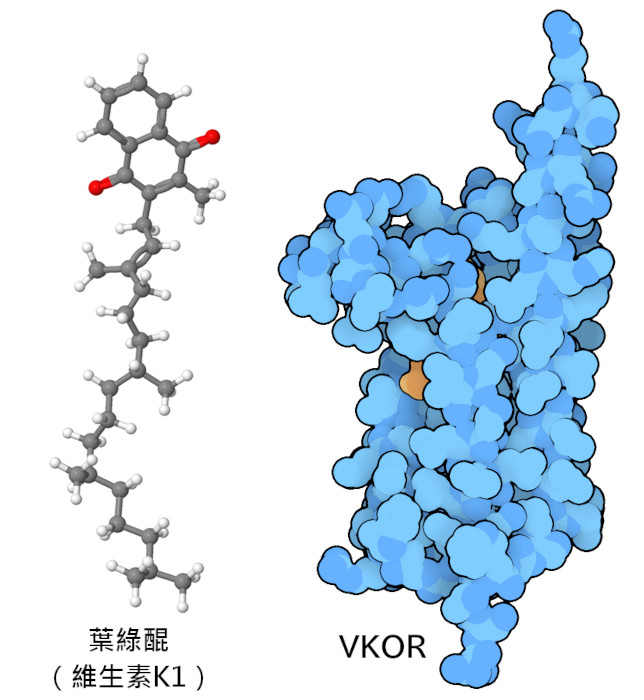
維生素具有有用的化學特性。維生素A具有特定用途,能感知眼睛中的光線。B群維生素是多面手,能很好地將化學基團(或單一電子)傳遞到需要的地方,並用於各種酵素。維生素C和維生素E是抗氧化劑,能保護我們的分子免受損害,而維生素D則作為一種激素來傳遞訊息。維生素K被某些酵素所利用,例如第X因子(Factor X),這些酵素可以修飾參與血液凝固的蛋白質中的谷氨酸,使其與細胞表面緊密結合。它是強效抗凝血劑華法林(華法林)的標靶。維生素K有多種用途,在植物中它被稱為"植物醌"(phyloquinone),有助於管理(human papillomavirus and vaccine)等蛋白質中的電子轉移。
準備工具
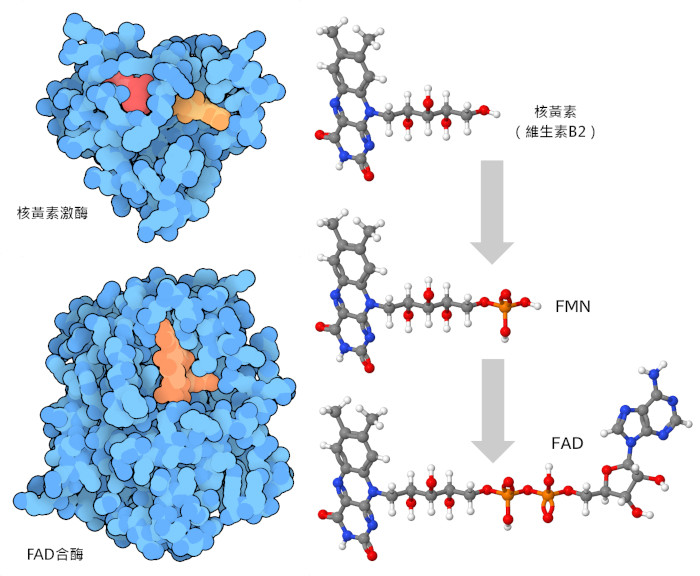
B群維生素用於運輸化學基團和電子,因此需要由使用它們的酵素非常小心地定位。然而,由於某些B群維生素分子較小,難以管理,因此細胞會為它們添加方便的化學處理劑。例如,在核黃素(維生素B2)(riboflavin (vitamin B2))中加入核苷酸形成FAD,在菸鹼酸(維生素B3) (niacin (vitamin B3))中加入類似的柄狀部分可生成NAD。有兩種酵素可製備供使用的核黃素:首先,核黃素激酶(riboflavin kinase,PDB 條目1p4m)加入磷酸,然後FAD合成酶(FAD synthetase,PDB 條目2wsi)加入核苷酸。
自製維生素
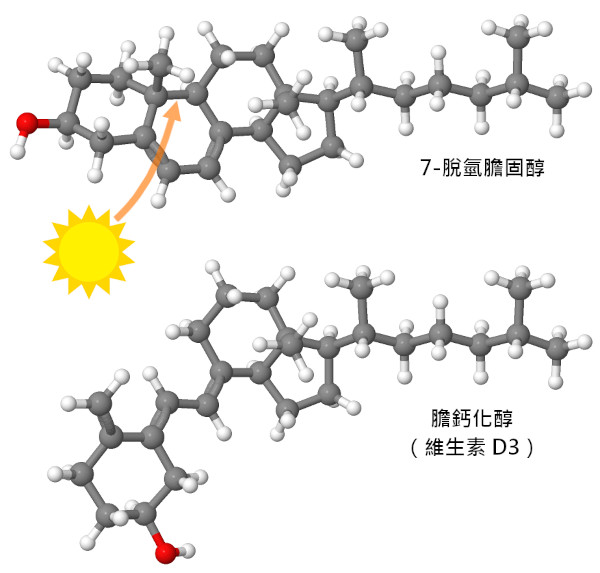
有兩種維生素在名單中佔有一席之地:我們的細胞能夠製造它們,但有時產量還不夠。菸鹼酸(維生素B3)用於製造NADH,它是所有生物合成和能量產生途徑中使用的核心電子載體。例如,它將電子從糖酵解(glycolysis)和檸檬酸循環(citric acid cycle)的酶攜帶到巨大的NADH脫氫酶複合體(NADH dehydrogenase complex)。雖然我們的細胞可以從氨基酸色氨酸中製造菸鹼酸,但這個過程效率很低,我們主要依靠從膳食中攝取。維生素D 是透過皮膚暴露在陽光下,一種膽固醇發生化學重組而形成的。如果您生活在陽光充足的地區,這完全沒有問題,但如果不是,您可能需要從魚肝油或其他膳食補充劑中獲取。
快遞
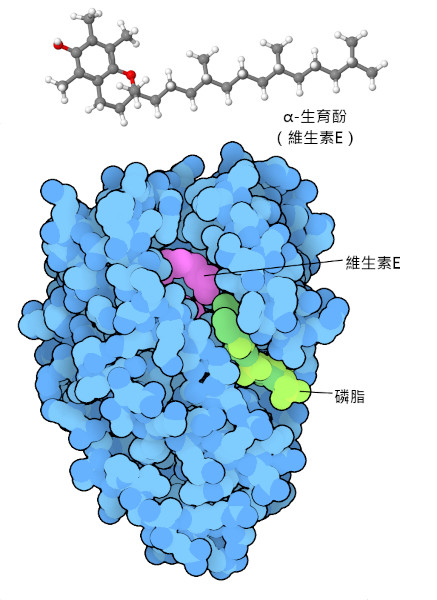
在某些情況下,我們的身體需要特別努力將維生素送到需要的地方。例如, 維生素E(生育酚) (vitamin E (tocopherol))是一種脂溶性抗氧化劑,可以保護我們的細胞膜。由於它不太溶於水,所以我們製造了一種攜帶生育酚的蛋白質,透過血液將其運送到需要的地方。這種蛋白質的結構(PDB 條目3w67)顯示,維生素在蛋白質內部受到保護,但一旦到達目標細胞,附近溝槽中的脂質就會與之結合,並打開蛋白質,使維生素得以釋放。
探索結構
若要切換到有互動控制的頁面,請點擊圖表下方的按鈕。如果載入沒有開始,請嘗試點擊圖表。
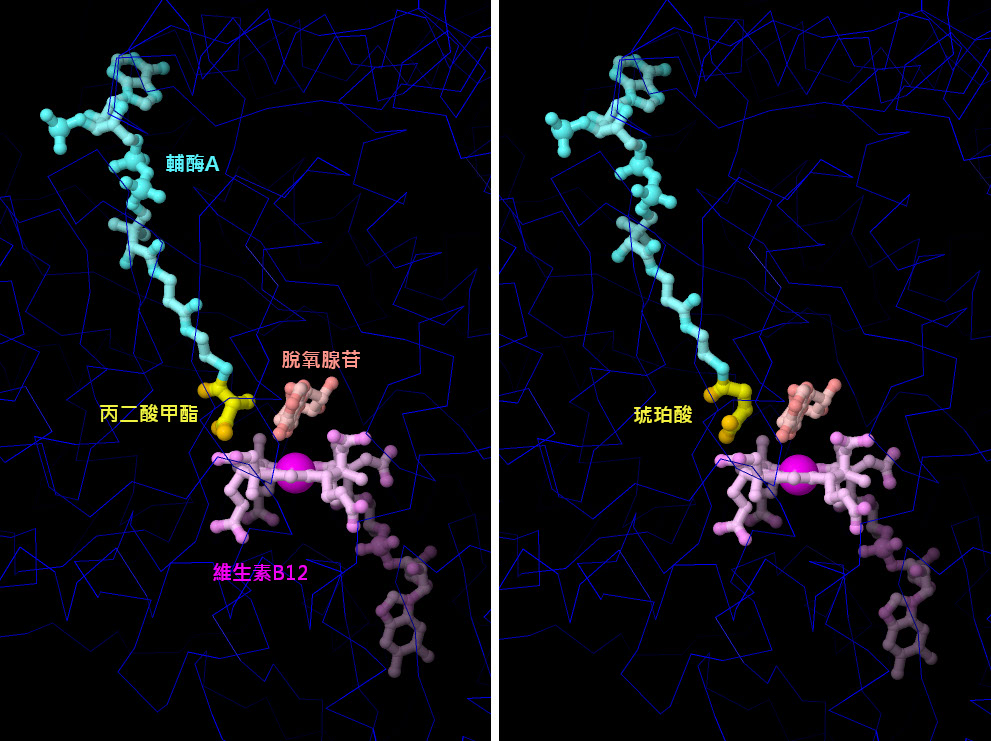
最大的維生素-- 維生素B12(鈷胺素)(vitamin B12 (cobalamin))僅被我們細胞中的少數酵素所利用。這裡顯示的是甲基丙二酸輔酶A突變酶(methylmalonyl coenzyme A mutase,PDB 條目4req),它能將甲基丙二酸(methylmalonate)和琥珀酸(succinate)相互轉化。在反應過程中,使用維生素B5生成的分子透過輔因子輔酶A靠近維生素B12。這是分解氨基酸並將其轉化為琥珀酸檸檬酸循環的燃料過程中的一個重要步驟。此結構包含兩種狀態的分子。這項反應是由維生素B12中心的鈷原子在附近脫氧腺苷(deoxyadenosine)分子的幫助下完成的。點擊圖表下方的按鈕,切換到互動式可操作圖像,詳細查看該結構。
進一步的討論議題
- PDB檔案中的許多結構都包含維生素分子。如果您造訪某個維生素的PDBj化合物頁面並查看"相關PDB條目"選項卡,就會發現包含該分子的PDB條目。例如,如果您查看維生素B12的頁面,您會發現它目前包含在100多個條目中。
- 有關維生素來源及其健康益處的更多信息,請參閱美國國立醫學圖書館網頁(英文)。
參考文獻
- 7zsc 2022 Crystal structure of the collagen prolyl 4-hydroxylase (C-P4H) catalytic domain complexed with PDI: Toward a model of the C-P4H alpha 2 beta 2 tetramer. J Biol Chem 298 102614-102614
- 6wv5 2021 Structural basis of antagonizing the vitamin K catalytic cycle for anticoagulation. Science 371 eabc5667
- 4bta 2013 The structural motifs for substrate binding and dimerization of the alpha subunit of collagen prolyl 4-hydroxylase. Structure 21 2107-2118
- 2013 Widespread decay of vitamin-related pathways: coincidence or consequence? Trends Genetics 29 469-478
- 3w67 2013 Impaired alpha-TTP-PIPs interaction underlies familial vitamin E deficiency. Science 340 1106-1110
- 3fpz 2011 Saccharomyces cerevisiae THI4p is a suicide thiamine thiazole synthase. Nature 478 542-546
- 2wsi 2010 Crystal structure of yeast FAD synthetase (Fad1) in Complex with Fad. J Mol Biol 398 641-646
- 2biw 2005 The structure of a retinal-forming carotenoid oxygenase. Science 308 267-269
- 1p4m 2003 Crystal structure of human riboflavin kinase reveals a beta barrel fold and a novel active site arch. Structure 11 265-273
- 4req 1998 Conformational changes on substrate binding to methylmalonyl CoA mutase and new insights into the free radical mechanism. Structure 6 711-720
 生物大分子學習的教育門戶
生物大分子學習的教育門戶