276点击化学Click Chemistry
了解蛋白质和核酸的结构,使我们有能力通过使用抑制剂阻断它们或用非天然的化学基团进行修饰以达到控制它们的目的。这是以结构为导向的药物发现的基础,目前许多重要的治疗药物都是通过这种方法发现的。然而,最大的挑战之一是生物分子具有复杂的形状,与它们结合的分子必须具有类似的特定形状。今年的诺贝尔化学奖被授予了三位研究人员,他们率先采用模块化的化学方法,帮助研究人员合成具有所需形状和特性的各种分子。
分子型乐高积木
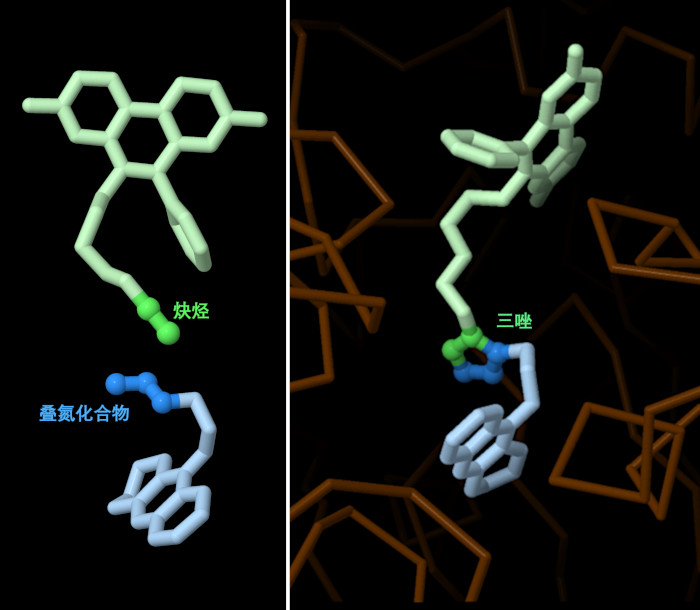
点击化学(click chemistry)允许研究人员通过连接模块化前体来构建定制分子。建立这些联系的诀窍是找到通常不反应但可以在适当条件下"点击"在一起的化学基团。Sharpless和Meldal实验室独立地发现,使用铜作为催化剂,具有叠氮基(azide)的化合物可以与具有炔烃(alkyne)的化合物连接。当它们反应时,这两个化学基团形成一个特有的五元环三唑(triazole),连接两个分子。
让酶来选择
令人惊讶的是,Sharpless实验室已经表明,一种酶可以在不需要铜的情况下进行这种相同的反应。这两个分子都与蛋白质结合,使叠氮基和炔烃接近并促进反应。在他们的经典实验中,他们将多对带有叠氮基或炔基的前体添加到乙酰胆碱酯酶(acetylcholinesterase)中,发现该酶只连接了最好的一个。使用这种方法,该酶产生了一种抑制剂,其结合比任何其他先前已知的非共价抑制剂更紧密,如此处显示的PDB条目1q83 的化合物所示。这种反应也发生在活细胞中,探针和传感器可以与细胞中的蛋白质相连。Bertozzi实验室开发了一系列对细胞友好的点击反应,例如,通过将炔烃嵌入紧张的分子环中来消除对有毒铜催化剂的需求。
古怪的建筑风格
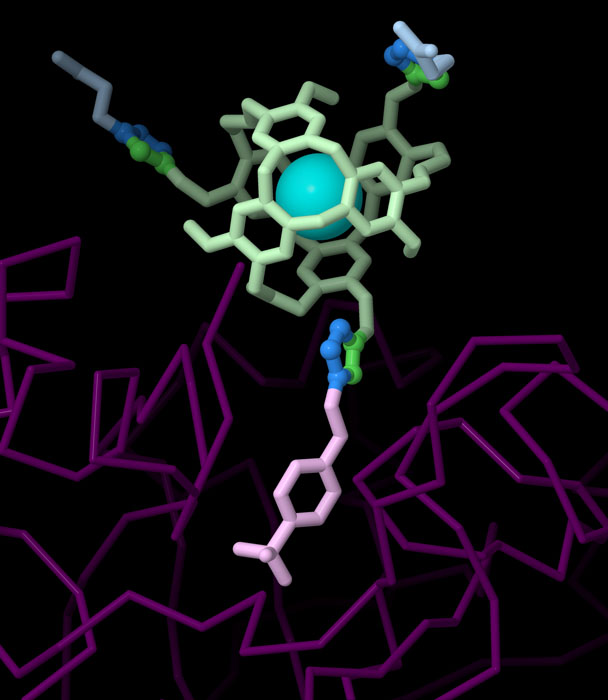
点击化学是合成化学中使用的一组方法的核心。点击化学被广泛用于组合化学,许多元素在不同组合中的效力都可以被快速研究。它也被用作一种有针对性的合成方法,以实现研究人员所希望的梦想分子。这里介绍的分子(PDB条目3cyu)被设计为一个生物传感器。顶端的球形隐烷(cryptophane)有一个点击反应的烷基分子,可以捕获氙原子(xenon atoms),这被认为是核磁共振成像中有用的对比剂。底部的叠氮化物部分是一种分子,能与目标酶碳酸酐酶 II(carbonic anhydrase II)特异性结合。
探索结构
要切换到有互动控制的页面,请点击图表下面的按钮。如果加载没有开始,请尝试点击图表。
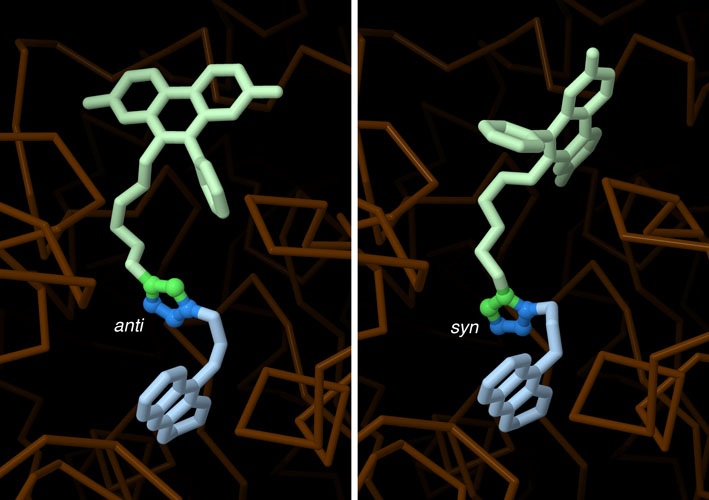
叠氮化物和炔烃前体之间的点击化学可以产生两种略有不同的三唑,即反(anti)和顺(syn)类型,这取决于它们在反应过程中如何相互排列。当使用铜作为催化剂时,大多数三唑类化合物具有反构型,两个连接的前体从五元环上向相反方向延伸(PDB条目1q84)。然而,在上述由乙酰胆碱酯酶催化的反应下,前体大多并排排列形成顺式三唑(PDB条目1q83)。正如预期的那样,生化测试表明,这种顺式化合物与酶的结合比反化合物更紧密。按下图片下方的按钮,可以切换到互动式可操作的图片,并仔细观察两者的结构。
进一步的讨论议题
- 许多点击化学抑制剂被收录在PDB档案中,可以通过RCSB PDB高级搜索中的Chemical Sketch Tool查找。例如,搜索SMILES字符串 "CN1C=C(C)N=N1"。
- 与乙酰胆碱酯酶结合的炔烃和叠氮前体可以在PDB条目5eih中查看。
参考文献
- 3cyu 2008 Structure of a 129Xe-cryptophane biosensor complexed with human carbonic anhydrase II. J Am Chem Soc 130 6942-6943
- 2005 Chemistry in living systems. Nat Chem Biol. 1 13-21
- 1q83, 1q84 2004 Freeze-frame inhibitor captures acetylcholinesterase in a unique conformation. Proc Natl Acad Sci U S A 101 1449-1454
- 2003 The growing impact of click chemistry on drug discovery. Drug Discov Today 8 1128-1137
- 2002 Click chemistry in situ: Acetylcholinesterase as a reaction vessel for the selective assembly of a femtomolar inhibitor from an array of building blocks. Angew Chem Int Ed 41 1053-1057











