303: 烯醯輔酶 A 羧化酶/還原酶(Enoyl-CoA Carboxylases/Reductases)
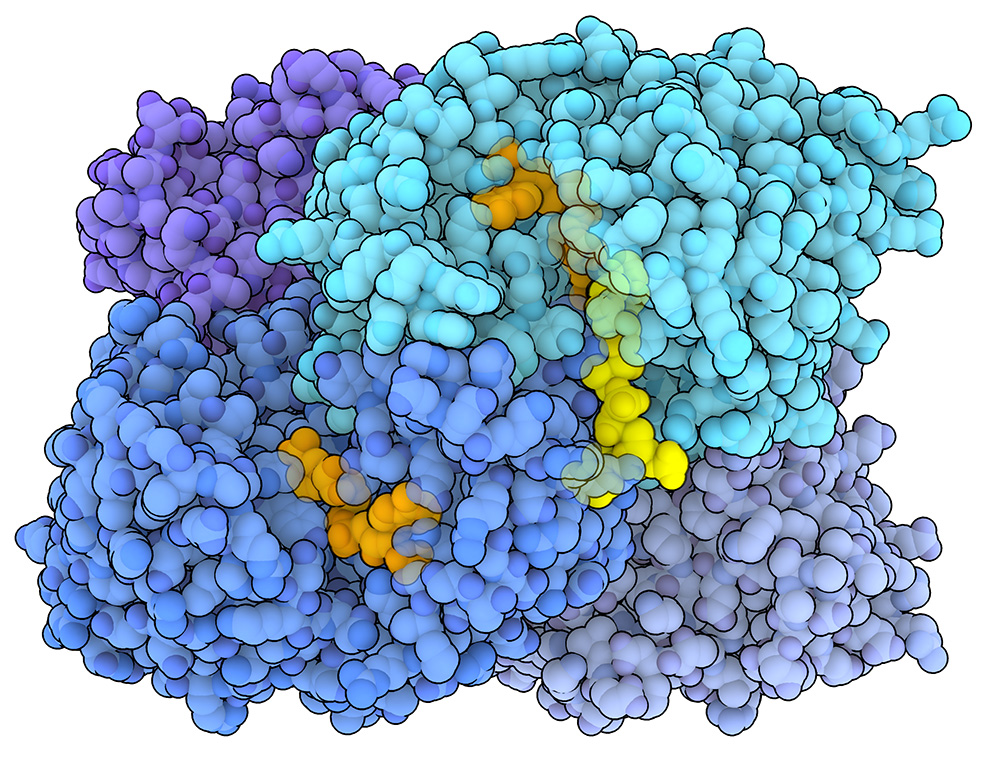
這篇文章的中文譯本尚未發布。請參閱PDB-101上的英文原文。

這篇文章的中文譯本尚未發布。請參閱PDB-101上的英文原文。
本文是由RCSB PDB的PDB-101提供的《當月的分子》2025年3月的文章的中文翻譯。請參考我們的條款和條件頁面。


還有VR、3D眼鏡
和遊戲





帶有VR(虛擬現實)的分子觀察器

為生物學學習提供的查看生物分子三維結構的在線服務!

用紙來製作蛋白質分子模型

蛋白質結構百科全書,含有PDB收錄的生物高分子的信息

以前的活動和講習會資料

記憶訓練遊戲和貪吃蛇遊戲

關於新型冠狀病毒感染(COVID-19)

PDBj
[日本蛋白質結構數據庫]
{
"header": {
"minimamHeightScale": 1.0,
"scalingAnimSec": 0.3
},
"src": {
"spacer": "/share/im/ui_spacer.png",
"dummy": "/share/im/ui_dummy.png"
},
"spacer": "/share/im/ui_spacer.png"
}