258: 糖質コルチコイド受容体とデキサメタゾン(Glucocorticoid Receptor and Dexamethasone)
この記事は、2021年1月に定量生物医学ラトガース研究所(Rutgers Institute for Quantitative Biomedicine)の主催で開催された1週間の集中合宿「生物医学における科学コミュニケーション」(Science Communication in Biology and Medicine)の一環で、ジェナ・アブヤド(Jenna Abyad)、タンビ・バノータ(Tanvi Banota)、ザッカリー・フリッツ(Zachary Fritz)、アレクサンドリア・ロー(Alexandria Lo)により執筆され、描かれたものです。
SARSコロナウイルス2型感染症と戦う
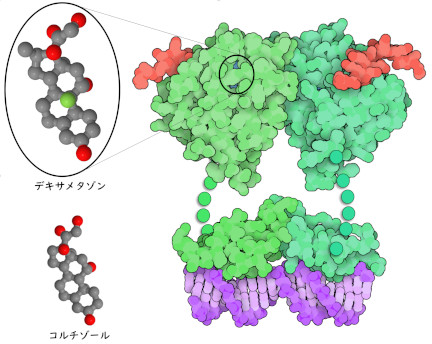
糖質コルチコイド(Glucocorticoid、グルココルチコイド)の薬は炎症や自己免疫疾患を治療するため広く処方されており、最近ではCOVID-19(SARSコロナウイルス2型感染症)の重症患者の治療にも用いられている。COVID-19は、発熱や息切れなどの症状から、多臓器不全などの重い合併症への急速に進行する。重症患者は「サイトカインストーム」(cytokine storm)を経験するが、このときにはもはやコロナウイルスに対する炎症反応を抑えることはできず、サイトカイン(炎症の分子メッセンジャー)の異常な産生がさらなる合併症を引き起こしてしまう。臨床試験では、糖質コルチコイド受容体に結合する強力な抗炎症薬であるデキサメタゾン(dexamethasone)を低用量で投与することにより、COVID-19入院患者の死亡率が低下したことが示されている。
移動中の受容体
糖質コルチコイドは、エストロゲン受容体(estrogen receptor)とともに核内受容体の仲間(ファミリー)に属している。これはリガンド結合ドメイン(ligand-binding domain)、DNA結合ドメイン(DNA-binding domain)、トランス活性化ドメイン(transactivation domain)という3つの部分で構成されている。ヒトの場合、この受容体のリガンドとして最もよくあるのがストレスホルモンの一つコルチゾール(cortisol)である。受容体がコルチゾールに結合すると、受容体の構造が変化し細胞質から核へと移動する。核内では、標的DNA配列に結合し遺伝子発現に影響を与えることができる。糖質コルチコイド受容体は活性化補助因子(coactivator)とも相互作用し、遺伝子発現のしくみをさらに調整することができる。受容体は柔軟なリンカーでつながれたいくつかのドメインで構成されているので、ドメインの構造は別々に決定された。デキサメタゾンに結合したリガンド結合ドメインの構造はPDBエントリー1m2z、DNAに結合したDNA結合ドメインの構造はPDBエントリー1gluのものを示す。トランス活性化ドメインはここに示していない。これらのドメインがすべて一緒になり、コルチゾールの結合によって引き起こされる最初のメッセージが伝達される。
過剰な炎症
薬であるデキサメタゾンの構造は天然のコルチゾールの構造と非常によく似ている。このことにより、デキサメタゾンは糖質コルチコイド受容体にぴったりと結合し、同じように体内の炎症を解消する遺伝子発現の変化を引き起こす。この活性のため、デキサメタゾンはCOVID-19の治療において特に効果的である。なぜなら、コロナウイルスによる損傷はウイルス自体によるものだけではなく、制御できない炎症によるものでもあるからである。ところが、デキサメタゾンの抗炎症効果は、使い方や時期を誤ると害をおよぼしかねない。COVID-19の初期段階において、身体はウイルスを撃退するために免疫系を動員する必要があるので、初期の重症ではない患者にデキサメタゾンを使うと、うかつにも患者の状態を悪化させてしまうかもしれない。
デキサメタゾンの服用:それは複雑
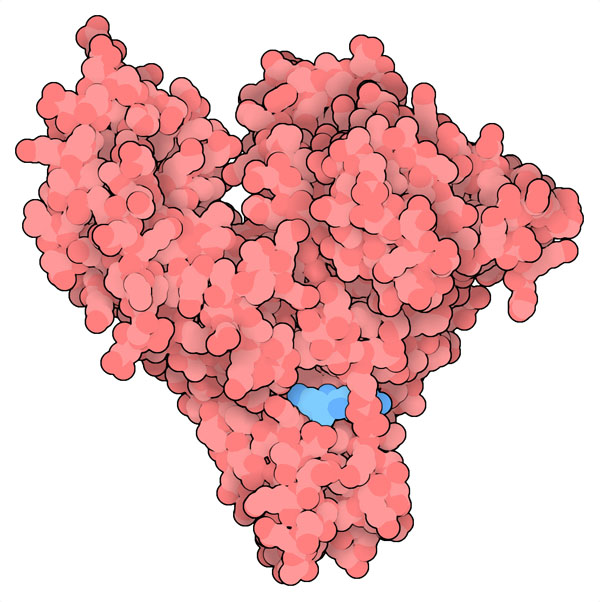
血清アルブミン(serum albumin)は血漿の中で最も豊富に見られるタンパク質だが、デキサメタゾンも他の薬やホルモンと同様にこの血清アルブミンによって身体全体に運ばれる。ところがこのタンパク質に関する因子のため、COVID-19に関連する炎症を治療するときに安全で効果的となるようデキサメタゾンを投与するのは難しい。例えば、糖尿病の患者では、タンパク質中の重要なアミノ酸に対して糖化(glycation)の過程を経て糖分子が結合していることがよくある。こうなると薬のタンパク質への結合が妨げられことがある。イブプロフェン(ibuprofen)のような一般的鎮痛剤なども血清アルブミン上にある同じ結合部位を使い競合するので、同時に服用するとデキサメタゾンの輸送が妨げられる。さらに、肝臓病、栄養失調、高齢などのCOVID-19の危険因子に加え、ウイルス自身も患者の血清アルブミン濃度を下げることがある。この複雑な事情により、内科医が血中におけるデキサメタゾンの遊離:結合の相対比を見積もり、薬の毒性増加、副作用、薬効の低下を招く可能性について判断するのは難しくなっている。
構造をみる
対話的操作のできるページに切り替えるには図の下のボタンをクリックしてください。読み込みが始まらない時は図をクリックしてみてください。
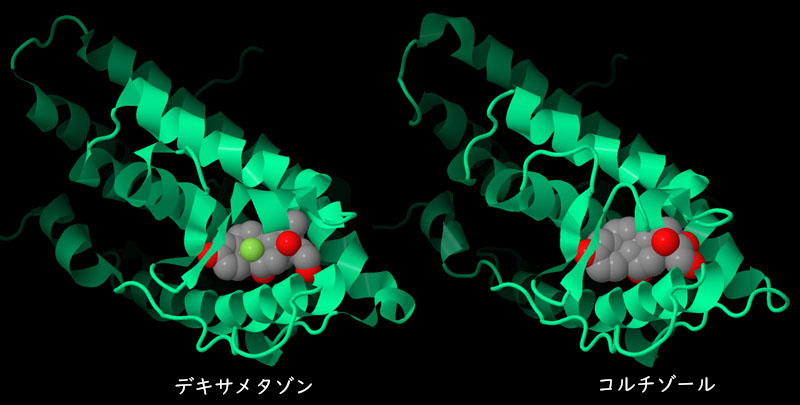
デキサメタゾンが結合した構造(左、PDBエントリー1m2z)とコルチゾールが結合した構造(右、PDBエントリー4p6x)の両方についてリガンド結合ドメインの構造が得られている。これらのリガンドは構造が非常によく似ていて、糖質コルチコイド受容体の同じ窪みに結合する。リガンドは原子種ごとに色分けした球で、糖質コルチコイド受容体は緑のリボンモデルで示している。これらの構造をより詳しく見るため、図の下のボタンをクリックし対話的操作のできる図に切り替えてみて欲しい。
理解を深めるためのトピックス
- 今月の分子の記事「インターフェロン」(interferon)には、ウイルス感染に応答してつくられるサイトカインの例が挙げられている。
- コロナウイルスの構造生物学についてより詳しく学びたいのであれば、RCSB PDBのPDB-101 - コロナウイルス関連資料(英語)を確認してみて欲しい。
- COVID-19の治療に関する推奨治療薬ガイドラインについてより詳しく学びたいのであれば、アメリカ国立衛生研究所(NIH)の治療ガイドライン(英語)を参照のこと。またPDB-101 COVID-19 - 分子の詳細に関するカリキュラムモジュール(英語)も参照して欲しい。
- 糖質コルチコイド受容体のような核受容体についてより詳しく学びたいのであれば、今月の分子の記事エストロゲン受容体(estrogen receptor)やビタミンD受容体(vitamin D receptor)を参照してみて欲しい。
参考文献
- 6xk0 2020 Molecular determinants of vascular transport of dexamethasone in COVID-19 therapy. IUCrJ 7 1048-1058
- 4p6x 2014 Structures and mechanism for the design of highly potent glucocorticoids. Cell Res. 24 713-726
- 1glu 1991 Crystallographic analysis of the interaction of the glucocorticoid receptor with DNA. Nature 352 497-505
- 4k2c 2013 Structural mechanism of ring-opening reaction of glucose by human serum albumin. J Biol Chem 288 15980-15987
- 4k2c 2013 Structural mechanism of ring-opening reaction of glucose by human serum albumin. J Biol Chem 288 15980-15987
- 2014 Comprehensive Overview of the Structure and Regulation of the Glucocorticoid Receptor. Endocrine Rev 35(4) 671-693
- 2013 The biology of the glucocorticoid receptor: New signaling mechanisms in health and disease. J Allergy Clin Immunol 132(5) 1033-1044
- 2013 The five Rs of glucocorticoid action during inflammation: ready, reinforce, repress, resolve, and restore. Trends Endocrinol Metab 24(3) 109-119
- 2020 Steroids in COVID-19: An overview. Cleve Clinic J Med. DOI:10.3949/ccjm.87a.ccc05 Epub ahead of print.
- 2001 Novel glucocorticoid receptor coactivator effector mechanisms. Trends Endocrinol Metab. 12(3) 122-126
- 2002 Cell 110 93-105
- 2014 Structures and mechanism for the design of highly potent glucocorticoids. Cell Res. 24 713-726
- 1991 Crystallographic analysis of the interaction of the glucocorticoid receptor with DNA. Nature 352 497-505
- 2020 Molecular determinants of vascular transport of dexamethasone in COVID-19 therapy. IUCrJ 7 1048-1058
 の生体高分子学習ポータルサイト
の生体高分子学習ポータルサイト 









