203: アミノペプチダーゼ1とオートファジー(Aminopeptidase 1 and Autophagy)
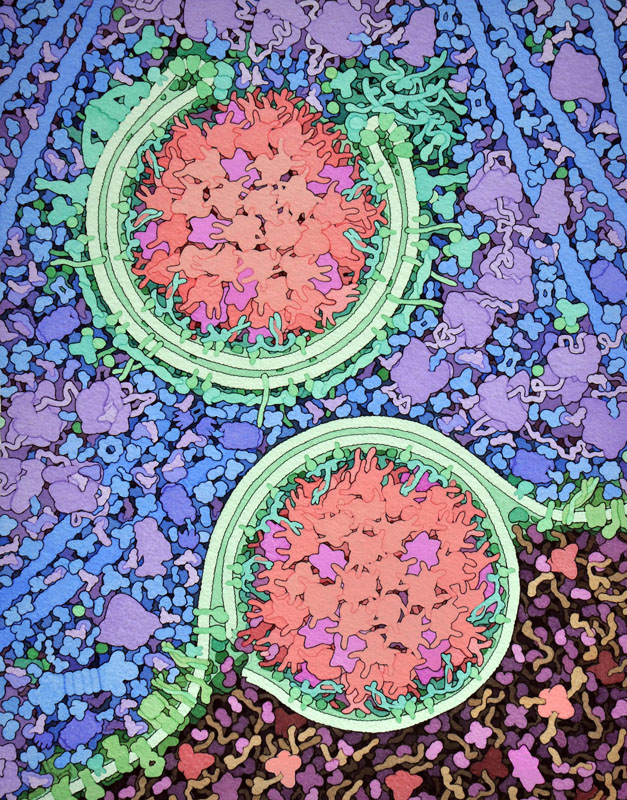
細胞は常に変化していて、必要な時に新たな分子をつくり、使い終わるとそれを分解する。プロテアソーム(proteasome)とエキソソーム(exosome)の系は一度に生体分子を一つずつをリサイクルするが、細胞にはオートファジー(autophagy)と呼ばれる、もっと大きなリサイクルを行う仕組みもある。この名称は「自分を食べる」ことを意味していて、それが細胞のやっていることそのものにもなっている。いらなくなったものを包み込み、内部の消化系であるリソソーム(lysosome)へと運ぶ。そこではあらゆるものが消化酵素のスープによって分解される。
オートファジーのはたらき
オートファジーは細胞でさまざまな欠かせない役割を果たしている。細胞が飢餓状態になると、オートファジーを使って自身が持つ細胞質の一部を飲み込み消化する。この自己共食いによって細胞自身を維持している。オートファジーは対象を限定することもでき、ミトコンドリアなどの細胞内小器官全体が損傷を受けたりもはや必要なくなったりした時にそれだけを取り囲んで廃棄することができる。生合成を行う時は選択的オートファジーも使って、消化酵素を細胞質からリソソームに輸送する。オートファジーは病気とさまざまなつながりがあるので関心は高い。例えば、オートファジーの機能不全に陥ると変性疾患の発生につながり、一方がん細胞ではオートファジーを過剰に働かせてがん細胞自身を生き残りやすくしている。
細胞質から液胞へ
選択的オートファジーの過程は酵母細胞で広く研究されている。酵母細胞の中央には大きな液胞があってリソソームの役割を果たしている。アミノペプチダーゼ1(aminopeptidase 1)という酵素がファゴフォア(phagophore)と呼ばれる二重の膜に囲まれ酵母の液胞へと運ばれる。図に示すように、この二重膜は酵素集合体の周辺すぐ近くに構築される。この構築過程を何十種類ものオートファジータンパク質が助けている。ファゴフォアの外側の膜は液胞膜と融合し、内側の膜は液胞内にあるリパーゼ(lipase)によって分解され、酵素が放出される。
アミノペプチダーゼの活性化
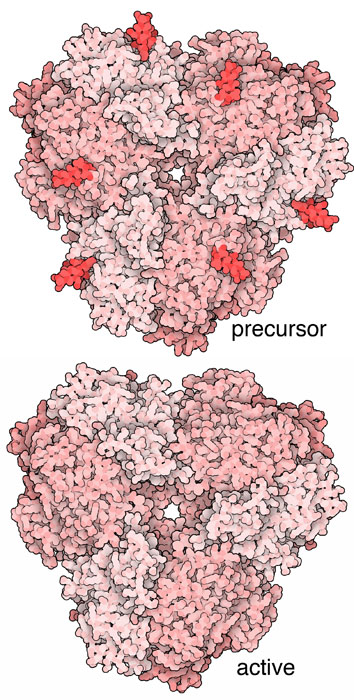
アミノペプチダーゼ1は、一端に小さなプロペプチドがついた不活性型前駆体(図示しているのはPDBエントリー5jh9)としてつくられる。このプロペプチドは隣の分子と相互作用して分子を凝集させ、また特定のオートファジー受容体タンパク質とも相互作用してファゴフォアを凝集体の周囲に形成させ、辺りにある酵素以外の細胞質はほとんど取り込まないようにしている。酵素が液胞の内側に入ると、プロペプチドが切り離され、活性型酵素(図示している構造はPDBエントリー4r8f)となる。
構造をみる
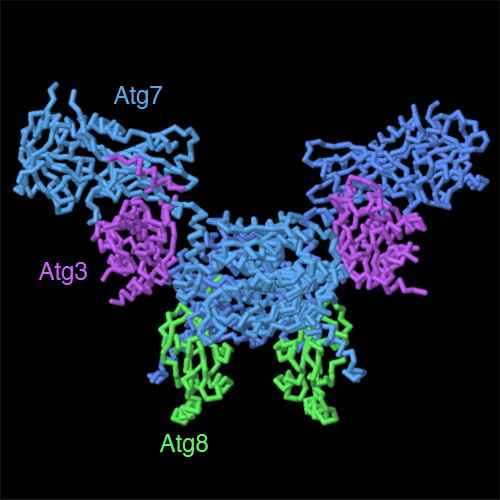
対話的操作のできるページに切り替えるには図の下のボタンをクリックしてください。読み込みが始まらない時は図をクリックしてみてください。
ファゴフォアを形成したり、リソソームや酵素の液胞などと融合したりするのに、何十種類ものタンパク質が協力し合っている。ここに示すタンパク質(PDBエントリー4gsl、3rui)は、アミノペプチダーゼ1をファゴフォア膜につなぎ止める受容体タンパク質の一種を活性化するのに関係している。酵母の場合、これらのタンパク質にはオートファジー関連タンパク質(Autophagy-related protein)を示すAtgという名前がつけられている。これらタンパク質のうち、Atg8はファゴフォア膜に見られるタンパク質で、Atg7とAtg3は脂質を付加してタンパク質を活性化するしくみの一部になっている。図の下のボタンをクリックして対話的操作のできる画像に切り替え、複合体をより詳しく見てみて欲しい。
理解を深めるためのトピックス
参考文献
- 2017 Structural biology of the core autophagy machinery. Current Opinion in Structural Biology 43 10-17
- 2016 An overview of macroautophagy in yeast. Journal of Molecular Biology 428 1681-1699
- 5jh9 2016 Structural basis for receptor-mediated selective autophagy of aminopeptidase 1 aggregates. Cell Reports 16 19-27
- 4r8f 2015 Structure of yeast Ape1 and its role in autophagic vesicle formation. Autophagy 11 1580-1593
- 4gsl 2012 Noncanonical E2 recruitment by the autophagy E1 revealed by Atg7-Atg3 and Atg7-Atg10 structures. Nature Structural and Molecular Biology 19 1242-1249
- 3rui 2011 Insights into noncanonical E1 enzyme activation from the structure of autophagic E1 Atg7 with Atg8. Nature Structural and Molecular Biology 18 1323-1330
 の生体高分子学習ポータルサイト
の生体高分子学習ポータルサイト 









