43: Srcチロシンキナーゼ(Src Tyrosine Kinase)
私たちの身体は細胞の民主主義国家である。各細胞が必要なものは個々それぞれ異なるが、全てが協同して働くことにより私たちを生かしてくれている。ご想像の通りがつくように、これには非常に多数の協力が必要とされる。細胞は、必要なものや将来の計画に関する情報を常に隣接する細胞とやりとりしている。お互いにメッセージを送り合っていて、ホルモン(hormone)、ケモカイン(chemokine、炎症性細胞遊走因子)などの分子メッセージが細胞間で行き来している。このメッセージは細胞膜に存在するタンパク質によって受け取られ、それが細胞内へと信号を伝える。そこで、非常に複雑なタンパク質の集まりが、各々のメッセージに応じた細胞内の適切な場所へ信号を中継している。
Srcの仕事
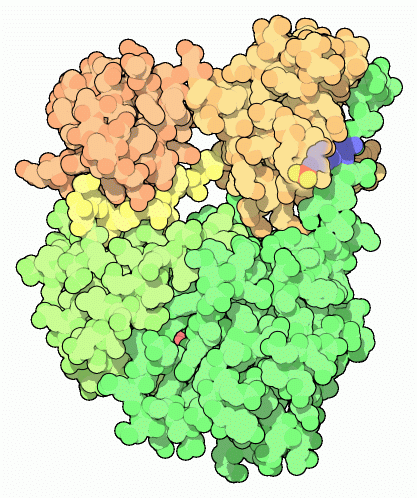
右図に示すSrcタンパク質(PDBエントリー 2src)は細胞の成長を制御するメッセージに特化した信号伝達タンパク質である。このタンパク質は細胞膜内部にだけ存在し、様々なタンパク質受容体からの信号を転送してタンパク質合成エンジンや細胞成長のスイッチをONにするのを助ける。Srcはチロシンキナーゼ(tyrosine kinase、チロシンリン酸化酵素)の一つで、タンパク質鎖中にある特有のチロシンアミノ酸にリン酸基(phosphate group)を付加することで信号を中継する。細胞構造、細胞間通信、細胞成長を制御する様々な種類のタンパク質にリン酸基を付加してスイッチをONにした後、それを解放して個々の仕事を実行させる。
冗長性
この複雑な信号伝達機構では、仮に通常の機構が動作しなくても他で代替する冗長的な仕組みが何重にも構築されている。何百種類ものタンパク質チロシンキナーゼが発見されているが、そのうちのいくつかはほとんどSrcと同じものである。実は、実験動物でSrcタンパク質の作用を阻害してもあまり影響が出ない。どうも他の類似タンパク質が、失われた機能の埋め合わせをすることができるようである。PDBには、Hckタンパク質(PDBエントリー 2hck)、Ablタンパク質(PDBエントリー 1opl)のようなSrcと似たタンパク質がいくつか登録されている。通常、これらのタンパク質は次々と行き交うメッセージを監督し、その指示に従って私たちは生き、成長し、修復を行っている。多くの場合、このタンパク質の機能が失われても比較的小さな影響で済むが、もしタンパク質の活性が過剰になると、悲惨な結果となる。
src がん遺伝子
Srcタンパク質をコードしているDNAはがん遺伝子(oncogene)として知られている。なぜなら、この遺伝子はがんの発生と大いに関係のある遺伝子だからである。src がん遺伝子はがんと関連していることによって発見された。ニワトリに腫瘍を引き起こす「ラウス肉腫ウイルス」(Rous sarcoma virus)はSrcの通常型に似た「v-Src」(virus Src、ウイルスSrc)と呼ばれるタンパク質をニワトリの細胞に注入する。v-Srcは細胞のSrc(c-Src)とは異なり、常に活性状態にある。Srcの作用受ける多くのタンパク質に対しリン酸基を付加し続け、成長するための信号を絶えず確実に送信し続ける。これはがんを招き、細胞はとどめなく成長して腫瘍になる。
変異がタンパク質を常時活性型に変える変異であった場合、通常型Srcおよびこの類似がん遺伝子タンパク質における変異がヒトのがんでよく見られる。現在、この面倒を起こすキナーゼを止め、通常の成長制限を再構築する方法が模索されている。イマチニブ(imatinib、商品名 グリベック Glivec、Gleevec)という薬はその中の注目すべき成功例の一つである。これはAblタンパク質の作用を阻害する働きがあり、このタンパク質が変異しているがんの治療に効果がある。
多くの可動部分
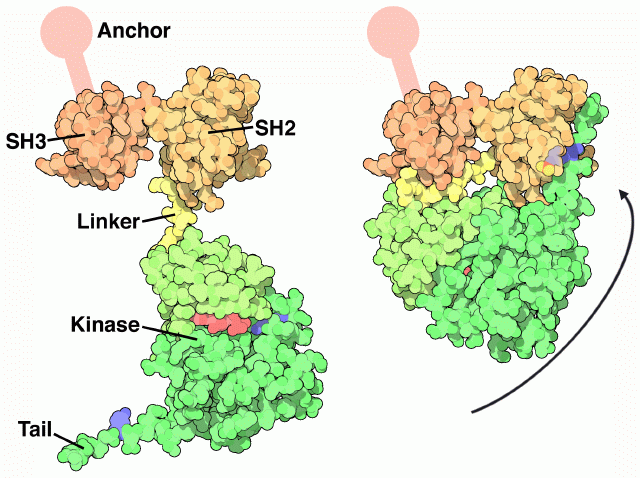
Srcは大きな関節が曲がるような動きを経てスイッチが入ったり切れたりする。上図右側に示した結晶構造(PDBエントリー 2src)は不活性状態の構造を示している。これが左に示すように開くと活性型タンパク質となる。Srcタンパク質は一連の機能部分がつながった1本のタンパク質鎖でできている。一方の端からもう一方の端まで見ていくと、固定化断片(anchoring segment、結晶構造では見えていない)、SH3ドメイン、SH2ドメイン、柔軟な結合領域、キナーゼドメイン、そして最終尾部がある。
この各部分とも機能にとっては欠かせない。まず左側の活性型を見て欲しい。SH3ドメインにはタンパク質鎖をつかむ小さな溝がある。そして、そこにつかんだタンパク質鎖にキナーゼドメインがリン酸基を付加できるよう、SH3ドメインはキナーゼドメインに十分接近した場所に来る。リン酸基はATP(図では赤色で示した部分)によって提供される。右の不活性型では巧みな方法で活性を止めている。自身をしっかりと折りたたみ、短い結合領域でSH3ドメインを阻害して他のタンパク質が結合できないようにしている。この不活性化する変化において重要なのは尾部にあるチロシン(図では青で示した部分)である。このチロシンはリン酸化されるとSH2ドメインの中に結合し、複合体全体をくっつけて閉じてしまう。チロシンからリン酸基が除去されると、尾部は解放されて分子全体が開き、SH3の結合部位阻害は解除されて、キナーゼ活性部位に接触できるようになる。
構造を見る
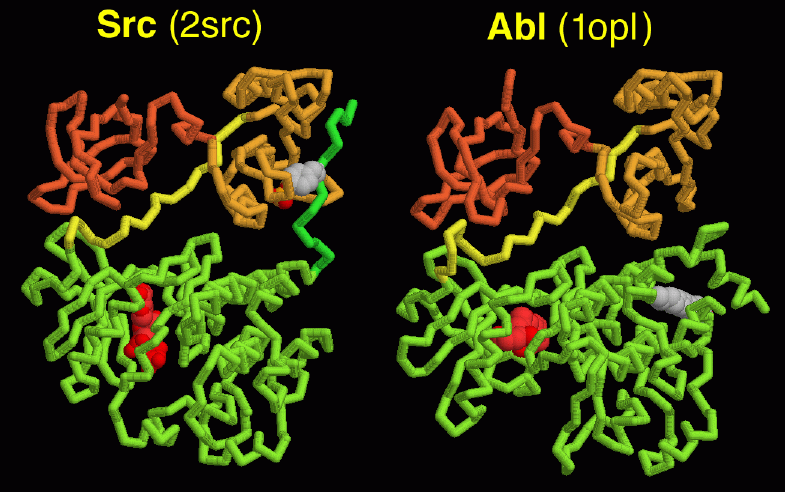
がん遺伝子タンパク質を探索する時、PDBエントリー 2src が良い出発点となるだろう。これはSrcの不活性型で、しっかり締まった球形に折りたたまれている。構造のキナーゼ活性部位(赤色部分)にはヌクレオチドが結合していて、キーとなるトリプシン(鎖の527番残基、分子右側)にはリン酸が付加されている。またHckタンパク質(PDBエントリー 2hck)を見るのもいいだろう。これはほとんどSrcと同じタンパク質である。また、全長ではSrcやHckより長いAblタンパク質断片をPDBエントリー 1opl で見ることができる。これはSrcやHckとは少し違っていて、閉じた型を安定化させるのに尾部を使わない。この構造には、活性部位に結合した薬剤分子(赤色)と深い窪みに結合した脂質(灰色)も含まれている。
なお 2hck や 1opl には2つの鎖が含まれているので、構造を見る時はA鎖だけを選択して見るようにすればいいだろう。
以下の参考文献・サイトもご参照ください。
- 1996 Regulation, Substrates and Functions of Src. Biochimica et Biophysica Acta 1287 121-149
- 2000 Src Family Tyrosine Kinases and Growth Factor Signaling. Experimental Cell Research 254 1-13
- Srcチロシンキナーゼ…Srcタンパク質とそのファミリーとの関係についての説明がInterProに記されています。
 の生体高分子学習ポータルサイト
の生体高分子学習ポータルサイト 









