215: アスパラギン酸カルバモイル転移酵素(Aspartate Transcarbamoylase)
細胞は組み立てラインを使ってアミノ酸や核酸のような必須分子を作ることがよくある。反応過程の各段階を担当する酵素は並んで一緒にはたらき、それぞれが異なる特定の化学反応を行なって、環境下で利用できる最初の原料から複雑な分子を作り上げる。この組み立てラインは慎重に調整されていて、必要な時にだけその分子が作られるようになっている。この調整は管理の手間をあまりかけずに行われることが多い。通常はラインの最初の段階を担当する酵素が最終産物の現在量を検知し、十分な量に達すれば自身のはたらきを止め、それによって組み立てライン全体も止まる。このしくみはフィードバック阻害(feedback inhibition)と呼ばれており、アスパラギン酸カルバモイル転移酵素(aspartate transcarbamoylase)の研究がこのしくみの解明に役立った。
二つの状態
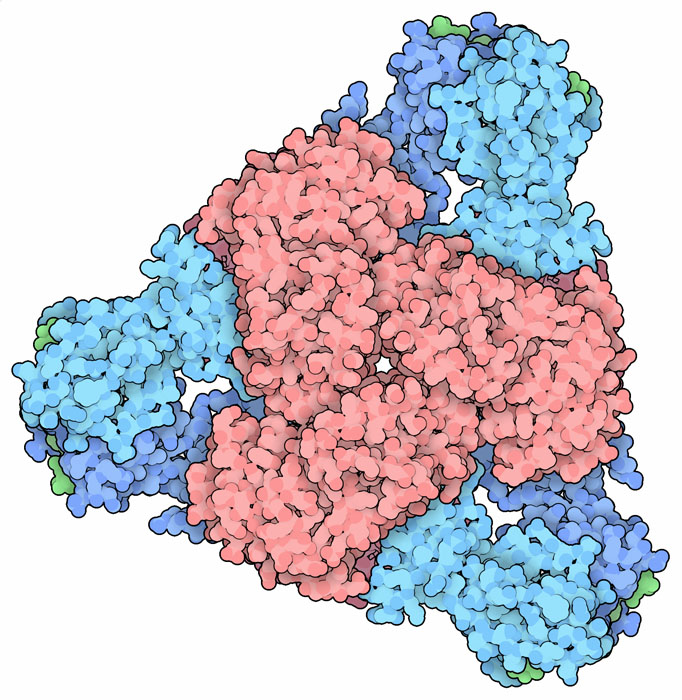
アスパラギン酸カルバモイル転移酵素(Aspartate Transcarbamoylase、ATCアーゼ)は、DNAやRNAに含まれるヌクレオチドの材料となるピリミジン環(pyrimidine ring)をつくる一連の反応のうち初期段階の反応を行う。初期の研究で、大腸菌のATCアーゼはピリミジン環を持ったヌクレオチドの一種CTP(シチジン三リン酸)の濃度によって制御されていることが分かった。生化学データに基づき、不活性なT状態(tense state、緊張状態)とR状態(relaxed state、緩んだ状態)の二つの状態をあらわしたモデルが提案された。そして分子の構造から、6つの触媒鎖が中央に配置されその周りを3組の制御鎖が取り囲んでいる大きな複合体となっていることが明らかになった。通常、複合体全体としては不活性型になっているが、触媒鎖はヘモグロビン(Hemoglobin)を構成する4つの鎖と同じように協力し合っていて、最初の原料がいくつかの活性部位に結合するとR状態が安定化され、複合体全体がより活性化される。一方、CTPの濃度が上昇すると、CTPが制御鎖に結合し不活性なT状態が安定化する。その様子をPDBエントリー5at1でみることができる。
どこで制御するのか
通常、制御酵素は反応過程全体の中でも独特な最初の段階を進める役割を担っている。ピリミジンの合成は、ATCアーゼよりも一つ前の段階となるカルバモイルリン酸合成酵素(carbamoyl-phosphate synthase、CPSアーゼ)から始まる。この酵素は細胞内でよくみられる構築材料からカルバモイルリン酸を作る酵素である。ところが、このカルバモイルリン酸はアミノ酸の一種アルギニンを作る時にも使われる。CPSアーゼをたった一種類しか持たない細菌もいるので、この酵素をピリミジン合成の制御に使うのはあまりいい方法ではない。この場合、次の段階を行いピリミジン合成にしか使われないATCアーゼがピリミジン合成の制御に用いられている。私たちの場合、2種類のCPSアーゼを持っていて、一方がピリミジン合成にもう一方がアルギニン合成に使われている。そのため私たちの細胞ではCPSアーゼがピリミジン合成の制御に使われている。
私たちが持つピリミジン工場
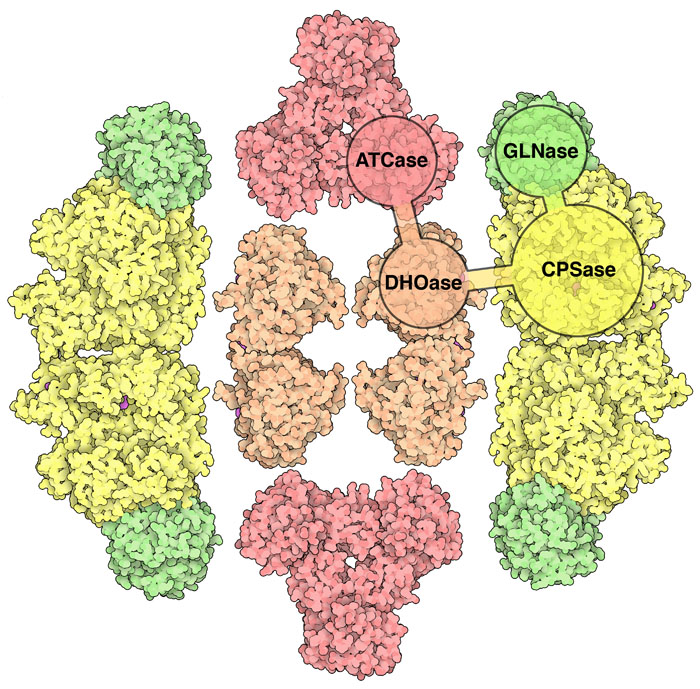
動物細胞において、ATCアーゼはCADと呼ばれる大きな多機能タンパク質の一部になっている。この巨大な複合体によって、ピリミジンを合成する3段階の反応が行われる。グルタミン依存性カルバモイルリン酸合成酵素(glutamine-dependent carbamoyl-phosphate synthase)に含まれる二つの酵素(GLNアーゼとCPSアーゼ)は一緒にカルバモイルリン酸を作る。ATCアーゼがアスパラギン酸をつなぎ、ジヒドロオロターゼ(dihydroorotase、DHOアーゼ)が閉じて環をつくって、ピリミジン塩基となる(PDBエントリー5dou、4c6i、5g1n)。ここに示すCPSアーゼはアルギニン合成に関わる酵素の一つで、CAD CPSアーゼと似ている。細菌もこれらの酵素をすべて持っているが、通常は個々にタンパク質をつくって別々に反応を進める。ヒトのATCアーゼ部分には触媒サブユニットだけが含まれていて、細菌の酵素複合体でみられる制御サブユニットは含まれないことに注目して欲しい。
構造をみる
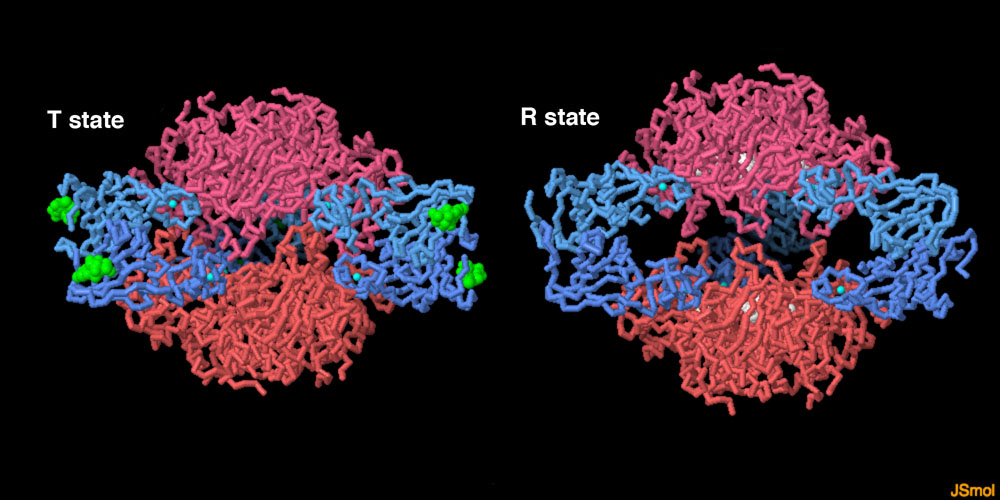
対話的操作のできるページに切り替えるには図の下のボタンをクリックしてください。読み込みが始まらない時は図をクリックしてみてください。
ATCアーゼの構造は何十個も決定されていて、T状態とR状態の両方の構造や、様々な基質・阻害剤と結合した構造が得られている。ここに示すそのうちの二つは、酵素が活性化される時に驚くべきアロステリック的な動きをすることを示している。T状態の構造(PDBエントリー4fyw)にはCTPが結合していて、R状態の構造(PDBエントリー1d09)には基質とよく似た阻害剤が活性部位に結合している。この二つの構造をより詳しく見るには、画面の下のボタンをクリックし対話的操作のできる画像に切り替えてみて欲しい。またGeisアーカイブではATCアーゼの状態についての芸術的描写を見ることもできる。
理解を深めるためのトピックス
参考文献
- 2017 Structural insight into the core of CAD, the multifunctional protein leading de novo pyrimidine biosynthesis. Structure 25 912-923
- 5g1n 2016 Structure and functional characterization of human aspartate transcarbamylase, the target of the anti-tumoral drug PALA. Structure 24 1081-1094
- 5dou 2015 Structure of human carbamoyl phosphate synthase: deciphering the on/off switch of human ureagenesis. Scientific Reports 5 16950
- 4c6i 2014 Structure, functional characterization and evolution of the dihydroorotase domain of human CAD. Structure 22 185-198
- 4fyw 2012 Metal ion involvement in the allosteric mechanism of Escherichia coli aspartate transcarbamoylase. Biochemistry 51 7128-7137
- 2011 Structure and mechanisms of Escherichia coli aspartate transcarbamylase. Accounts of Chemical Research 45 444-453
- 1d09 1999 Insights into the mechanisms of catalysis and heterotropic regulation of Escherichia coli aspartate transcarbamoylase based upon a structure of the enzyme complexed with the bisubstrate analogue N-phosphonacetyl-L-aspartate at 2.1 A. Proteins 37 729-742
- 5at1 1990 Structural consequences of effector binding to the T state of aspartate carbamoyltransferase: crystal structures of the unligated and ATP- and CTP-complexed enzymes at 2.6-A resolution. Biochemistry 29 7691-7701
 の生体高分子学習ポータルサイト
の生体高分子学習ポータルサイト 









