173: アクアポリン(Aquaporin)
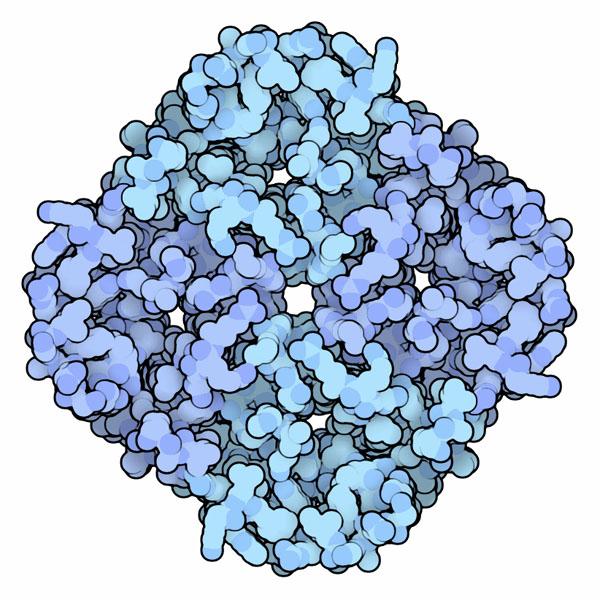
細胞膜には水分子が通らないようにする障壁がつくられており、極めて高い防水性がある。しかし、細胞によっては膜を越えて水が通れるようにする必要がある。例えば、腎臓(kidney)における老廃物の濃縮や眼の内圧は、水を慎重に制御することと関係している。これらの場合、細胞はアクアポリン(aquaporin)を使って、細胞における水を出入りを制御している。
1つの分子に4つのチャネル
アクアポリンは細菌からヒトまで幅広い生物でみられ、いずれも特徴的な構造を持っている。その特徴とは、同じ鎖が4つ集まり、それぞれのサブユニットの中央には1つずつのチャネルがあるというものである。後述するように、このチャネルにはタンパク質を通り抜けようとする水分子が1列に並んで行列をなしている。4つの鎖の中央にはチャネルより大きな穴があるが、ここには炭素が豊富なアミノ酸が並んでおり、恐らく細胞内では膜の脂質に入り込んでいると思われる。ここに示すアクアポリン(PDBエントリー 1fqy)は赤血球でみられるものである。ここには構造を示していないが、より最近になって解かれたより解像度の高い構造(PDBエントリー 3zoj)から、水だけを通しヒドロニウムイオンやヒドロキシイオンは通さないようにする上で、水チャネルの入口にあって電荷を持っている2つのアミノ酸が重要であることが明らかになった。
アクアポリンを対象とした薬の開発
アクアポリンは様々な種類の細胞で浸透圧を制御するのに欠かせない役割を果たしているので、この作用を妨げる方法を探し、緑内障(glaucoma)のような水に関係する病気の治療法を作り出すことができないか研究が行われている。アクアポリンは元々、赤血球において水銀が水の出入りを妨げる現象を観察することで発見されたものだが、残念ながら水銀は薬として使うには毒性が強すぎる。現在、特定の型のアクアポリンについて、その作用を妨げる新たな阻害剤を探し、これを薬として使う検討が進められている。
アクアグリセロポリン
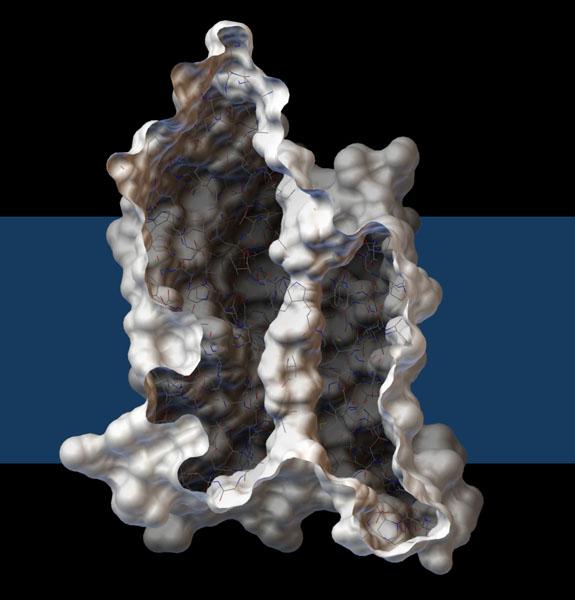
私たちは十数種類以上ものアクアポリンを持っていて、それぞれ異なる種類の細胞で違った役割を果たしている。通すものを水だけに強く限定しているものから、水以外のものも通すものまで様々である。ここに示すのはそのうちの一つ「アクアグリセロポリン」(aquaglyceroporin、PDBエントリー 1fx8)で、水とグリセリンを通すことができる。ここにはサブユニット1つだけを示しており、膜を貫通するトンネルが見えるよう一部を切り取ってある。チャネルの上端付近にくびれた箇所があることに注目して欲しい。この部分が通過できる分子の種類を制御している。なおこの図はPython Molecular Viewerで作成したものである。
構造をみる
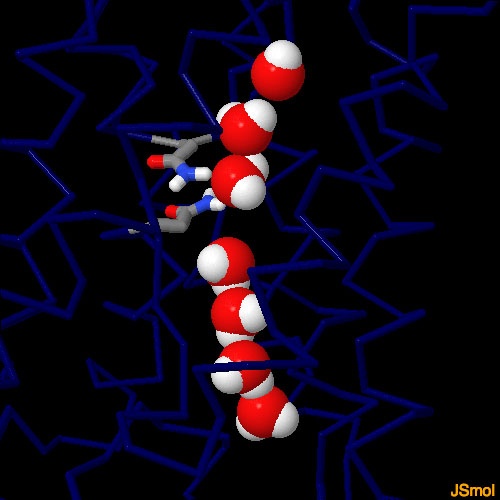
対話的操作のできるページに切り替えるには図の下のボタンをクリックしてください。読み込みが始まらない時は図をクリックしてみてください。
アクアポリンを貫通している水チャネルは深刻な問題を引き起こす可能性がある。なぜなら、水分子が並んでいると通常は「グロータス機構」(Grotthuss mechanism)によって分子から分子へプロトンが素早く伝わってしまうからである。もしこういったことが起これば大惨事となりうる。なぜなら、これにより細胞表面にある多くのポンプに動力を与えている電気化学勾配が使い果たされてしまうからである。アクアポリンは、水分子が特定の方向を向くようにすることでプロトンの通り道にとならないようにし、そのような事態を防いでいる。2つの特徴的なアミノ酸「アスパラギン」(asparagine)があって、これが中央の水分子1個(PDBエントリー 3zojの場合は2個)をつかんで、特定の方向を向かせている。この水はチャネルにならぶ他のアミノ酸と同調して、チャネルを通ろうとする行列に並んでいる前後の水分子と相互作用し、上流にある水をある方向に、下流にある水はその逆の方向を向かせる。図の下のボタンをクリックすると、水分子とそれらの向きを定めるアクアポリンのアミノ酸をみることができる。なおこの図は、PDBエントリー 1ymg の構造に、この構造では見えていない水素を追加して作成したものである。
理解を深めるためのトピックス
- PDBにはアクアポリンの構造が何種類か登録されている。それらがどれだけ似ているのかを、RCSB PDBのCompare Structuresなどの構造比較ツールを使って比較してみて欲しい。
- PDBに登録されているアクアポリンの多くは閉じた構造をしていて、アミノ酸が水チャネルを塞ぐ位置に来ている。これが活性状態における一つの開閉過程を示したものであるのかどうかを明らかにするための研究が続けられている。
参考文献
- 1fx8 2000 Structure of a glycerol-conducting channel and the basis for its selectivity. Science 290 481-486 10.1126/science.290.5491.481
- 1fqy 2000 Structural determinants of water permiation through aquaporin-1. Nature 407 599-605 10.1038/35036519
- 1ymg 2004 The channel architecture of aquaporin O at 2.2 Angstrom resolution. Proceedings of the National Academy of Science USA 101 14045-14050 10.1073/pnas.0405274101
- 2006 The structure of aquaporins. Quarterly Reviews of Biophysics 39 361-396 10.1017/S0033583506004458
- 2012 Aquaporins in clinical medicine. Annual Review of Medicine 63 303-316 10.1146/annurev-med-043010-193843
- 3zoj 2013 Subangstrom resolution X-ray structure details aquaporin-water interactions. Science 340 1346-1349 10.1126/science.1234306
- 2014 Aquaporins: important but elusive drug targets. Nature Reviews Drug Discovery 13 259-277 10.1038/nrd4226
代表的な構造
- 1fqy: アクアポリン
- アクアポリンは水分子が細胞膜を通過するためのチャネルをつくっている。
 の生体高分子学習ポータルサイト
の生体高分子学習ポータルサイト 









