60: ユビキチン(Ubiquitin)
永遠に続くものは存在しない。実際、多くのタンパク質は数分しか持たない。そのため、私たちの細胞では絶えずタンパク質を作り続けている。その際、単一の作業を使ってタンパク質を作り、そして捨てている。例えば、転写制御因子(transcription regulator)や細胞分裂を制御するサイクリン(cyclin)のように信号伝達や制御に用いられるタンパク質は大変寿命が短く、それらが担う情報を運び終えると捨てられてしまう。また各用途に特化した酵素はそれぞれ必要な時にだけ作られ、時々刻々合成の必要なものが変化するのに細胞が追従できるようにしている。この計画的に廃棄していくやり方は無駄が多いように見えるが、このやり方によって常に変化する要求に各細胞が素早く対応できるようにしているのである。
古いものの排出
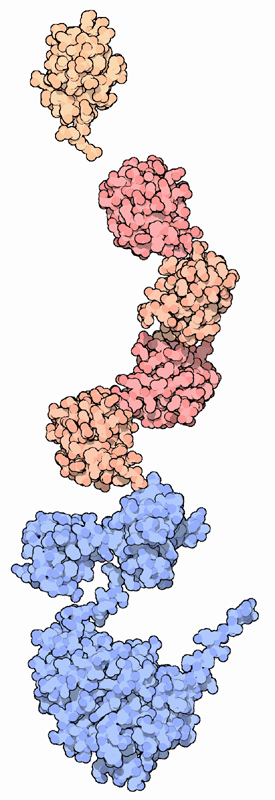
もちろん細胞は自分自身が持つタンパク質の破壊を制御し、確実に必要なくなったタンパク質だけを取り除く必要がある。小さなタンパク質であるユビキチン(ubiquitin)がこの仕事において中心的な役割を果たす。ユビキチンは要らなくなったタンパク質に付加され、細胞に解体の準備ができたことを伝達する。図示したように、ユビキチン分子の連なり(ピンクと黄褐色で示した分子、PDBエントリー 1ubq)が古いタンパク質に付加される。なおここに示した古いタンパク質はsrcタンパク質(青、PDBエントリー 2src)である。そして、ユビキチンは細胞の破壊機械に認識される。
どこにでもあるユビキチン
その名前が暗示しているように、ユビキチンは全ての真核細胞、身体全体の細胞に見られる。この年(2004年)のノーベル化学賞は、1980年にユビキチンの必須機能を発見した3人の科学者に贈られた。その後、ユビキチンはタンパク質廃棄における役割とは別に、細胞内外間のタンパク質輸送を指示するなどの他の役割もあることが明らかになってきた。ユビキチンを短鎖や長鎖でつなげたり、分子との結合に別の型を使ったりして、様々な信号がコードされているようである。ユビキチンは重要な役割を果たしているため、生命進化の過程でほとんど変化してこなかった。そのため、酵母細胞、植物細胞、そして私たち自身の細胞で似た型のユビキチンが見つかる。なお、ユビキチンを遺伝的視点から見た追加情報を、欧州バイオインフォマティクス研究所(EBI)の「今月のタンパク質」(Protein of the Month)で見ることができる。
ユビキチン化
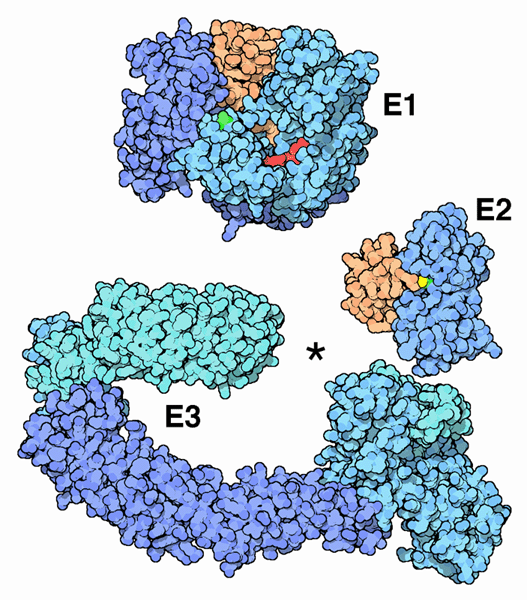
不要タンパク質の除去過程全体において巧妙な部分が、ユビキチンを適切なタンパク質にだけ付加されるのを確かなものにしている。いくつかの特別な酵素が細胞内のタンパク質をより分け、適切なものだけを取り出す。こういった酵素は3種類あり、それぞれE1、E2、E3と呼ばれている。図の上部に示しているE1酵素(PDBエントリー 1r4n)はユビキチンを活性化する酵素で、一連の過程を開始させる。E1酵素はATP(赤)の力によって、ユビキチン(淡橙)の末端をE1酵素自身のシステインアミノ酸(緑、但しこの構造ではシステインがアラニンに変異している)に付加する。そしてE1は活性化したユビキチンをいくつかあるE2酵素のどれか1つに渡す。E2酵素はユビキチン接合酵素で、ここに示したのはPDBエントリー 1fxtの構造である。これらE2酵素は多数ある別のE3酵素と一緒に働いて要らなくなったタンパク質を認識し、ユビキチンを付加する。ここに示したE3酵素はPDBエントリー 1ldkと 1fqvの構造で、大きな留め金のような形をしている。ユビキチンを付加する対象のタンパク質はすき間(星印を示している位置)に結合する。酵素の左側はタンパク質を認識し、右側はE2が持ってくるユビキチンを転移できるようにしている。
総合的破壊
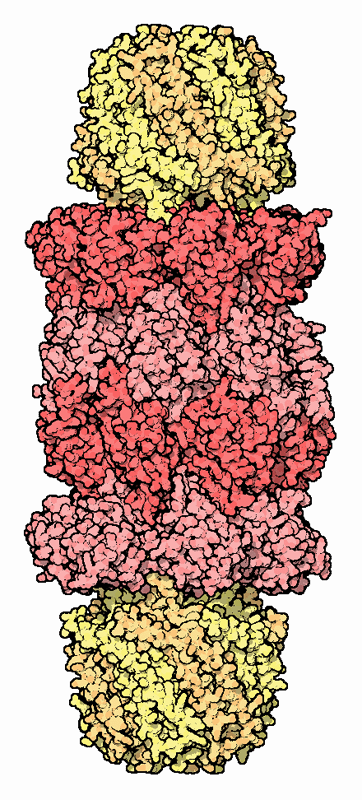
要らなくなったタンパク質は、少なくとも4個のユビキチン分子を付加された時点でプロテアソーム(proteasome)によって破壊される。プロテアソームは貪欲なタンパク質シュレッダーだが、この破壊機械は注意深く保護されているので細胞内にある通常のタンパク質はどれも到達することができない。ここに示したPDBエントリー 1fntのプロテアソームは筒状の形をしていて、活性部位を筒の内部に保護している。両端のふたはこの破壊容器に入るのを制御していて、ここに入ったタンパク質は3〜23個のアミノ酸で構成されるペプチド断片へと切断される。
構造をみる
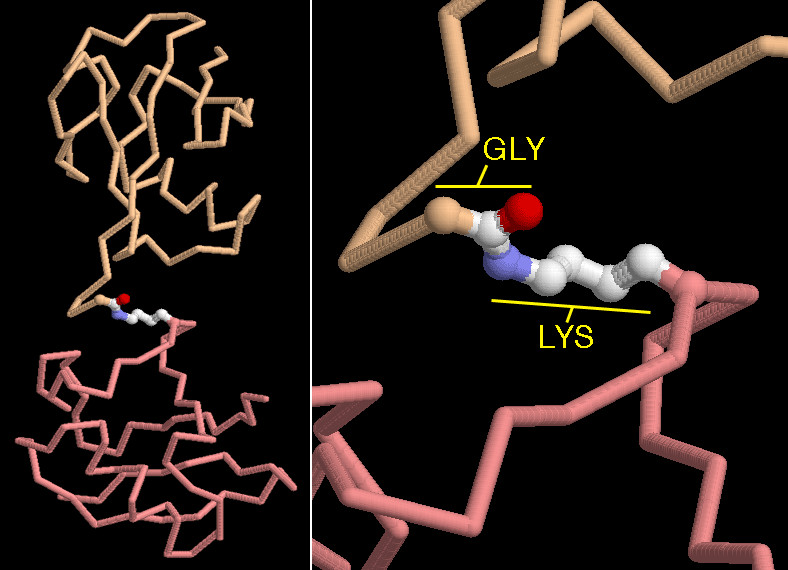
PDBエントリー 1f9jの構造は、どのようにしてユビキチン分子がつながって鎖になるのかを示している。結晶はテトラユビキチン(tetraubiquitin、4個のユビキチンがつながったもの)の状態になっているが、この構造では2個のユビキチン分子間の結合だけが見られる。よく近づいて見ると、独特の結合がA鎖の末端にあるグリシンアミノ酸とB鎖の途中にある148番のリジンアミノ酸の側鎖との間に見られる。
ユビキチンについてさらに知りたい方へ
以下の参考文献もご参照ください。
- 2002 Structural basis of ubiquitylation. Current Opinion in Structural Biology 12 822-830
- 2002 The ubiquitin-proteasome proteolytic pathway: destruction for the sake of construction. Physiological Reviews 82 373-428
- 2000 Ubiquitinin chains. Trends in Biochemical Sciences 25 544-548
代表的な構造
- 1ubq: ユビキチン
- A chain of ubiquitin molecules are added to obsolete proteins, indicating that they need to be destroyed. This structure includes a single ubiquitin molecule.
- 1f9j: tetraubiquitin
- A chain of ubiquitin molecules are added to obsolete proteins, indicating that they need to be destroyed. This structure includes four ubiquitin molecules connected in a chain.
- 1r4n: ubiquitin-activating enzyme E1
- Several enzymes are needed to recognize obsolete proteins and add ubiquitin to them. This enzyme is similar to E1, the enzyme that activates ubiquitin.
- 1fxt: ubiquitin-conjugating enzyme E2
- Several enzymes are needed to recognize obsolete proteins and add ubiquitin to them. This enzyme takes activated ubiquitin and attaches it to the protein.
- 1ldk: ubiquitin-ligase E3
- Several enzymes are needed to recognize obsolete proteins and add ubiquitin to them. This structure includes part of the enzyme E3, which recognizes obsolete proteins.
- 1fqk: ubiquitin-ligase E3
- Several enzymes are needed to recognize obsolete proteins and add ubiquitin to them. This structure includes part of the enzyme E3, which recognizes obsolete proteins.
- 1fnt: proteasome
- Proteasomes destroy obsolete and damaged proteins inside cells. This entry includes a proteasome with an 11S activator at each end.
 の生体高分子学習ポータルサイト
の生体高分子学習ポータルサイト 









