53: セルピン(Serpins)
私たちの細胞はしばしば危険な機械として働くよう強いられる。例えば、DNAやRNAを壊すヌクレアーゼ(nuclease)、炭化水素(carbohydrate)を壊すアミラーゼ(amylase)および関連する酵素、脂肪をかみ砕くリパーゼ(lipase)、タンパク質を分解するプロテアーゼ(protease、タンパク質分解酵素)といった様々な破壊のための機械を細胞は作っている。これらの破壊的酵素は大きな処理能力が必要とされ、食べ物に含まれる分子を実際利用できる断片へと分解する消化(digestion)に使われる。また、体内に侵入してくるウイルス(virus)や細菌(bacteria)に攻撃を加えるための防衛手段としても使われる。細胞内にある欠陥のある分子やもう使われなくなった分子を分解するのにも使われる。メッセージを受け取るとすぐに信号分子を活性化する信号伝達(signaling cascade)にも使われる。これらの酵素は適切な時と場所で使われることが不可欠であるが、もし遊離してしまうと災いを引き起こしうる。
プロテアーゼからの保護
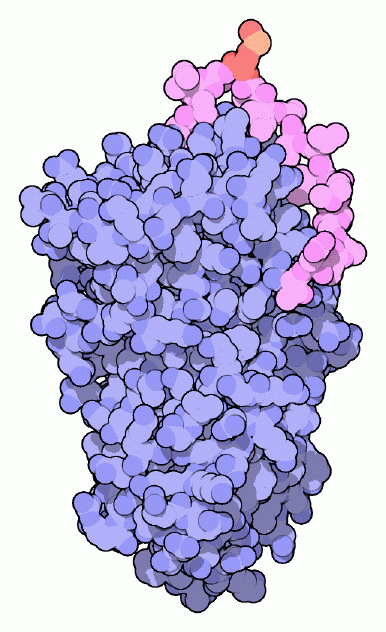
私たちの細胞はこの破壊的機械を制御するため、機械の活動を阻害し危険を取り除く多くのタンパク質も作っている。セルピン(serpins)はこのような分子の中の一グループで、特定のセリンプロテアーゼ(serine protease)を見つけ出して破壊するよう設計されている。セルピンという名前は何かギリシャ神話に由来するもののように聞こえるが、そうではなくセルピンの持つ機能〜セリンプロテアーゼ阻害剤(SERine Protease INhibitor)〜に由来している。ここに示したのはα1-アンチトリプシン(alpha1-antitrypsin、PDBエントリー 1psi)の例である。これは血流中に見られ、タンパク質を切断する酵素エラスターゼ(elastase)から周囲の組織を守っている。好中球(neutrophil、白血球の一種)は炎症(inflammation)が発生している部位にエラスターゼを分泌し、これが結合組織を分解することにより血液細胞が入って防衛や修復といった仕事をできるようにしている。セルピンは隣接する領域を保護し、エラスターゼが身体中に広がらないようにしている。
プロテアーゼを捕らえる
セルピンはネズミ捕りのような分子で、餌と揺れ動く腕で獲物の捕獲を成し遂げる。このタンパク質は準安定性タンパク質である。これは、活性型では部分的にしか安定とならないが、プロテアーゼを見つけるとずっと安定な型になることができる、ということを意味している。重要な部分は赤紫色で示した柔軟な環状領域である。この環状領域にある1つのアミノ酸が餌として用いられる。α1-アンチトリプシンの場合、この餌として用いられるアミノ酸はメチオニン(methionine、赤と橙で示した部分)である。後述するように、プロテアーゼがこの餌に食いつくと捕獲され破壊される。
セルピンの巣
ヒトのセルピンは30種類以上研究されており、それぞれが異なる必須の仕事を担っている(それらが多数PDBには登録されている)。その多くは血液中で見られ、うち何種類かは血液凝固(blood clotting)の過程を制御している。アンチトロンビン(antithrombin)は血栓形成の際トロンビン(thrombin)の作用を制限し、アンチプラスミン(antiplasmin)は血栓が溶解する時プラスミン(plasmin)の作用を制限している。また別のセルピンは補体系(complement system、細菌感染から私たちを守る仕組み)で使われるプロテアーゼ(protease)の作用を制御する。なお、この分子の様々な仲間に関する記述が欧州バイオインフォマティクス研究所(EBI)の「今月のタンパク質」(Protein of the Month)があるので参照のこと。
セルピンが失敗する時
セルピンが正常に機能しなくなると、深刻な問題を引き起こしうる。よく見られるのは次に述べる2種類の問題である。セルピンが不具合を起こすと、固有の対象を阻害できなくなり放置されたプロテアーゼが暴れ回ってしまうかもしれない。この現象は肺気腫(emphysema)で起こっており、α1-アンチトリプシンが損傷してエラスターゼが肺の結合組織を破壊してしまうことで問題を引き起こしている。セルピンが働かなくなる原因の一つは喫煙で、餌として使われるメチオニンアミノ酸が修正されてしまうことがある。また、代わりに使われるセルピンの独特な捕獲機構(後述)がまた別の問題を引き起こす可能性がある。環状領域が破壊された後、別のセルピンと結合し、かさ高い凝集体となりうる。もしこの凝集体が神経細胞内でできると、神経の機能が阻害され認知症(dementia)を引き起こすかもしれない。
罠を旅する
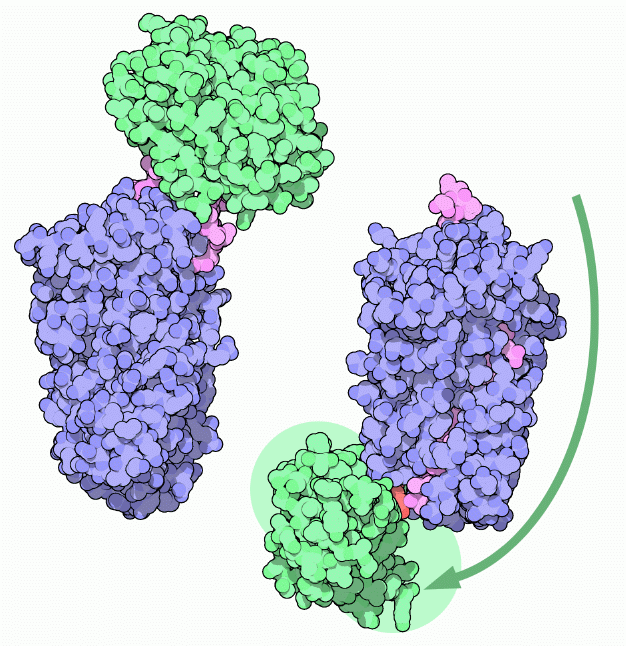
セルピンの柔軟な環状領域は、反応中心ループ(reactive center loop)として知られる、餌と罠になる部分である。緑で示したプロテアーゼは餌に食いつき、通常の切断反応を始める。上図左の構造(PDBエントリー 1k9o)はセルピンと結合した直後のトリプシンを示している。プロテアーゼ(トリプシン)中にある反応性セリンは環状領域を攻撃し、鎖と結合を形成して切断を行う。その後、通常であれば水分子を使いプロテアーゼは切断対象分子から解放される。ところが、不幸なトリプシンは自身を解放するよりも前にセルピンの制御下に置かれてしまう。切断されて自由に動けるようになった柔軟な環状領域は、セルピンの側面にある十分な大きさのある溝にしまい込まれ、それに伴ってプロテアーゼは反対側の側面へと引っ張ってこられる(上図右の構造、PDBエントリー 1ezx)。トリプシンは残りの反応を行って自身を解放できると思うかもしれない。ところが、セルピンの鎖は側面の溝にしっかりつかまれ数個のアミノ酸しか出ていない状態で、これは解放反応を行うには短すぎるため、トリプシンはセルピンの底にくっついたまま動けなくなってしまう。そしてこれによってトリプシンの活性部位は変形し、活性を失ってしまう。またトリプシンは不安定化させられ、部分的に構造がほどかれた状態になってしまう。これは不具合のあるタンパク質を一掃する分子機械にとって分かりやすい標的となり、プロテアーゼと使い捨てのセルピン双方が破壊される。
構造をみる
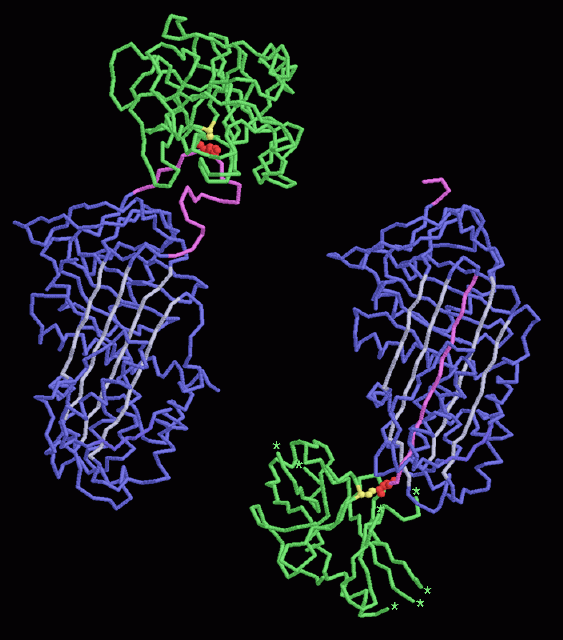
上図に示した2つの驚くべき結晶構造は、α1-アンチトリプシンの反応前後の様子を示している。左に示したPDBエントリー 1k9o はプロテアーゼが捕らえられる前のセルピン-プロテアーゼ複合体を示している。科学者たちは反応性セリンをアラニン(alanine、黄色)に変えた変異体プロテアーゼを使って罠に捕獲されていない複合体を見えるようにした。セルピン内に白で示した4本の長い並行鎖があることに注目して欲しい。上図右に示したPDBエントリー 1ezx は腕がしまい込まれた後の複合体を示している。環状領域が壊され、トリプシンははるばるセルピンの反対側へと引っ張ってこられている。トリプシンの中にあるセリン(黄色)はセルピンの中にあるメチオニン(赤)に結合している。壊され環状領域からできた鎖が4本の並行鎖の真ん中へどのようにしてしまいこまれたのかに注目して欲しい。またトリプシンが不安定化していることにも注目して欲しい。タンパク質鎖の多くは動きが多すぎるため結晶構造では見えていない。小さな星印は実験結果上の末端で、見えていない環状領域が続く部分を示している。
"セルピン" のキーワードでPDBエントリーを検索した結果はこちらで参照できます。
更に知りたい方へ
以下の参考文献もご参照ください。
- 2002 Serpin structure, mechanism and function. Chemical Reviews 102 4751-4803
- 2002 Serpins: Finely balanced conformational traps. IUBMB Life 54 1-7
- 2001 The serpins are an expanding superfamily of structurally similar but functionally diverse proteins. Journal of Biological Chemistry 276 33293-33296
- 1994 The serpin superfamily of proteinase inhibitors: Structure, function and regulation. Journal of Biological Chemistry 269 15957-15960
 の生体高分子学習ポータルサイト
の生体高分子学習ポータルサイト 









