219: 液胞型ATPアーゼ(Vacuolar ATPase)
通常私たちは、酸が危険な腐食性のものと考えるが、細胞は注意深く制御された酸をさまざまな有用物として利用している。例えば、私たちの細胞は特別な受容体を使ってLDL(low density lipoprotein、低密度リポタンパク質)のような分子を血液から集め、小胞の中に取り込み、小胞を酸性化してそれを放出する。リソソーム(lysosome)は酸性化されて、損傷を受けたりもう要らなくなったりした分子の分解を助ける。酸性は時折細胞外でも役に立つ。例えば骨細胞はミネラルが豊富な骨を分解し再構築するのに酸を使う。
プロトンポンプ
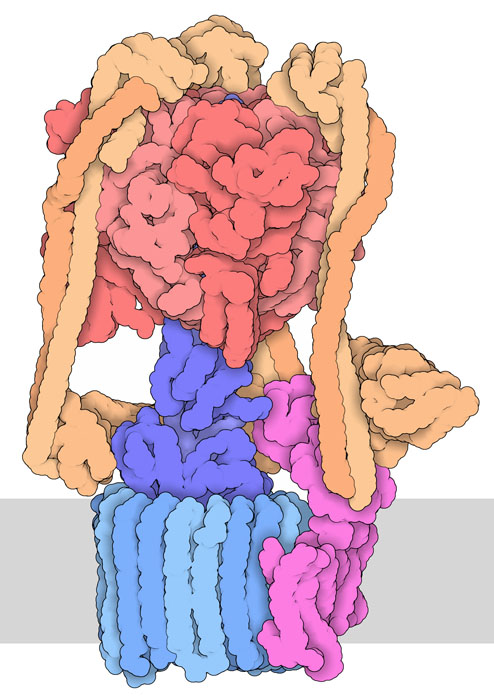
細胞が酸性度を制御する一つの方法は、ポンプを使って細胞内のプロトン(水素イオン)濃度を上げるという方法である。液胞型ATPアーゼ(vacuolar ATPase、V-ATPアーゼ)はATPのエネルギーで動作するプロトンポンプ(ここに示すのはPDBエントリー5vox由来の構造)で、2つの回転モーターから構成されている。上部(ピンク色の部分)はATPで駆動するモーターで、濃い青色の部分を軸として回転する。そしてこの回転が2つ目のモーター(薄い青色と赤紫色の部分)を回転させ、膜を越えてプロトンが輸送される。残りのタンパク質鎖(オレンジ色の部分)は一緒になって複合体全体を支え、一方のモーターの回転が確実にもう一方のモーターに伝わり、回転動力として利用されるようにしている。
酸性の制御
もちろん、細胞はこれらのポンプを制御し、細胞内が酸性に偏り過ぎないようにしておく必要がある。驚くべきことに、V-ATPアーゼは必要なくなると複合体を二つに分解されて機能が抑えられる。ATPで駆動するモーターはプロトンの輸送するモーターと切り離され、処理は停止するのである。そして再び必要となると、2つのモーターが再びつながれ、ポンプは再び働き始める。
回転モーター
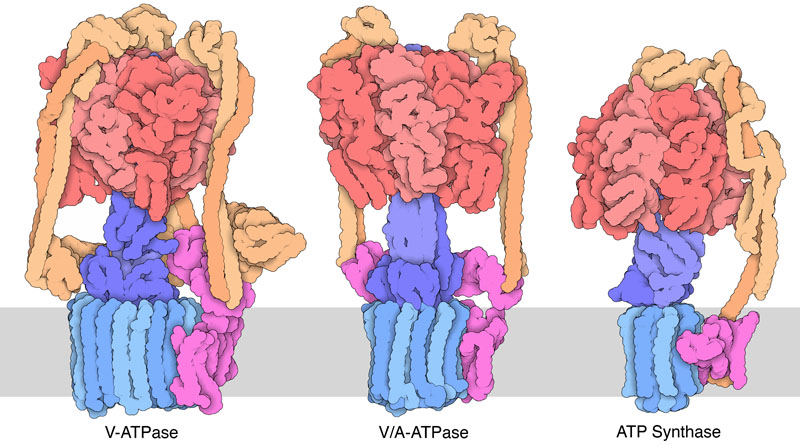
この種のつながった回転モーターは大変役に立つことが分かっていて、いくつかの種類がある。V-ATPアーゼは真核生物によってつくられ、酸性度を制御するのに使われている。ATP合成酵素(ATP synthase、PDBエントリー5ara)は私たちのミトコンドリアだけでなく細菌からも見つかっているが、その機能は正反対で細菌のものは膜結合部位を通るプロトンの流れを使ってATPをつくっている。V/A-ATPアーゼ(PDBエントリー5gar)はプロトンポンプやATP製造器といったさまざまな機能を持っている。また、ひとひねり加えプロトンの代わりにナトリウムイオンを使う回転モーターもある。
構造をみる
対話的操作のできるページに切り替えるには図の下のボタンをクリックしてください。読み込みが始まらない時は図をクリックしてみてください。
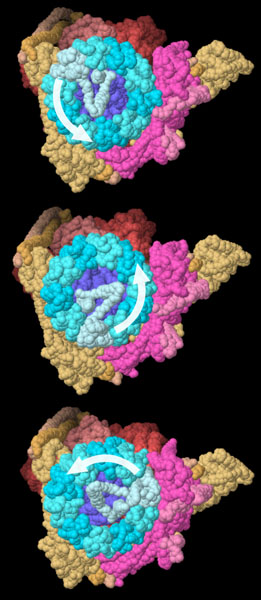
V-ATPアーゼは多くの可動部分を持つ複雑な分子機械なので、研究するのが難しいことは分かっていた。だが今日ではクライオ電子顕微鏡(cryoelectron microscopy)を使ってほぼ完全な構造が得られている。ここには酵母に由来するV-ATPアーゼの構造を示す。複合体の異なる3つの回転状態に関する構造が得られている(PDBエントリー5vox、5voy、5voz)。ここに示す図は分子を下から見上げたもので、プロトンをくみ入れる部分が回転する様子を示している。分子全体の回転をみるには、図の下のボタンをクリックし、対話的操作のできる画像に切り替えてみて欲しい。
理解を深めるためのトピックス
- V-ATPアーゼ、V/A-ATPアーゼ、ATP合成酵素ぞれぞれの環の中にある多くのサブユニットを比較してみよう。分子が一つのATPを分解または構築するのにいくつのプロトンが必要なのかについて、ここからどんなことが分かるだろうか。
- これまでV-ATPアーゼのさまざまな部分に関する原子構造が決定されており、これらはクライオ電子顕微鏡で得られた低解像度のモデルを構築する上で役に立った。V-ATPアーゼでPDBエントリーを検索し、そのような原子構造を探してみて欲しい。
参考文献
- 5vox、5voy、5voz 2017 Molecular basis for the binding and modulation of V-ATPase by a bacterial effector protein. PLoS Pathogens 13 e1006394
- 5gar 2017 Models for the a subunits of the Thermus thermophilus V/A-ATPase and Saccharomyces cerevisiae V-ATPase enzymes by cryo-EM and evolutionary covariance. Proceedings of the National Academy of Science USA 113 3245-3250
- 5ara 2015 Structure and conformational states of the bovine mitochondrial ATP synthase by cryo-EM. Elife 4 e10180
 の生体高分子学習ポータルサイト
の生体高分子学習ポータルサイト 









