201: イソプレン合成酵素(Isoprene Synthase)
植物が毎年10トンもの有機ガスを大気中に放出していると聞けば驚くかもしれない。このうちの約半分は、揮発性有機化合物のイソプレン(isoprene)である。世界中の森林で見られる樫、ヤマナラシ、ポプラ、ユーカリなどの高木で作られている。植物から発散されるイソプレンの量は相当なもので、日光を弱めてしまうほどである。これは、レオナルド・ダ・ビンチ(Leonardo da Vinci)が興味を持った青く美しいかすみをつくり、今日でも米国のブルーリッジ山脈やオーストラリアのブルーマウンテンのような風光明媚な場所で目にすることができる。
イソプレンの放出
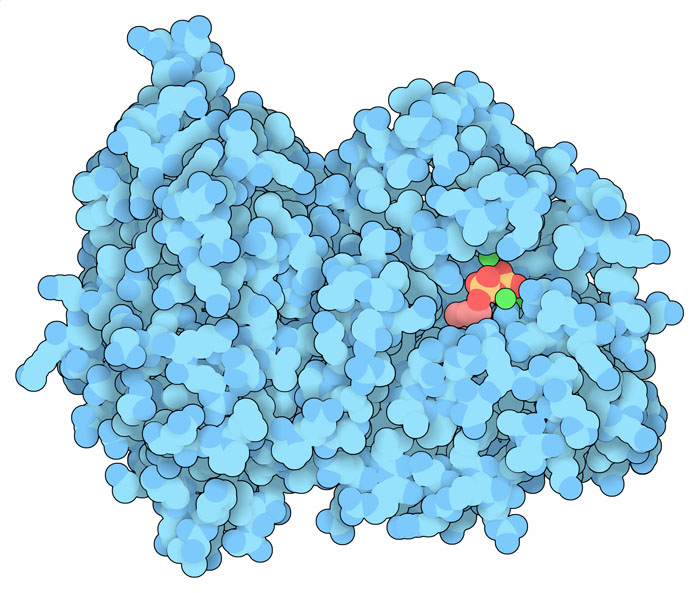
植物では、イソプレン合成酵素(isoprene synthase、ここに示すのはPDBエントリー3n0g)がジメチルアリル2リン酸(dimethylallyl diphosphate、DMAPP)を分解しイソプレンをつくっている。このDMAPPは、脂肪酸やステロイドホルモンなど多くのイソプレノイド(isoprenoid)をつくる材料となるものである。イソプレン合成酵素は金属イオンを使ってDMAPPからリン酸を取り除き、イソプレンを放出する。このイソプレンは大気中で起こる化学反応において重要な役割を果たしている。例えば、ヒドロキシラジカルや一酸化窒素に作用し、最終的にはオゾン濃度を増加させていることが分かっている。イソプレン合成酵素に関する理解が進むことにより、新たなタイプの酵素を設計し、人工プラスチックやゴムなどの工業産物を製造するための材料としてイソプレンをつくれるようになった。
葉の保護
葉が日光にさらされると表面温度は急速に変化するが、イソプレンは熱によってつくられる反応性の高い分子から葉を守っていると考えられている。植物にとって利のあるこの機能説明は、植物がイソプレン合成酵素を合成する量は季節により変動すること、木の先端部にある葉はより多くの日光にさらされるためよりたくさんのイソプレンをつくることなどいくつかの証拠によって裏付けされている。植物は光が当たっていないときでも、低濃度ではあるがイソプレンを放出している。そのためイソプレンは、草食動物に抵抗したり干ばつによるストレスの減らしたりするための防御機構としても働いていると考えられている。
構築材をつくる
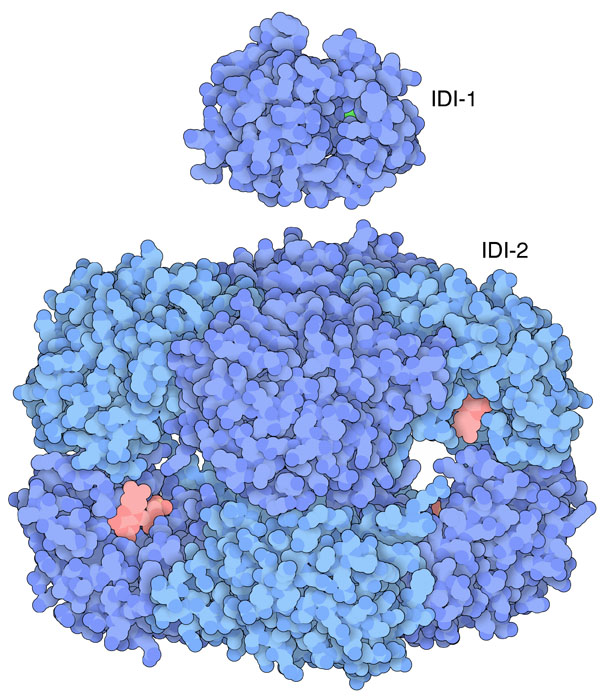
イソプレン前駆体のDMAPPとそれに似た分子のイソペンテニル2リン酸(isopentenyl diphosphate、IPP)は、あらゆる種類の生物で数々の重要分子をつくるのに使われる。その範囲はステロイドホルモンからユビキノン(ubiquinone)のような電子輸送体まで幅広い。これら2種類の分子のうちどちらが必要とされているかに応じて、イソプレン合成酵素はDMAPPとIPPとを相互に変換する。天然で知られている酵素には2種類の型がある。1型イソメラーゼ(PDBエントリー 1i9a)は相互変換を触媒するのに金属イオンを使うが、2型酵素(PDBエントリー 1p0n)の場合は同じことをするのにヌクレオチド補因子を使う。
構造をみる
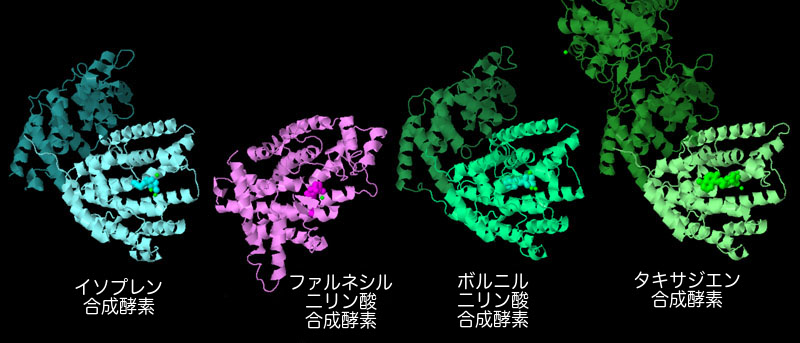
対話的操作のできるページに切り替えるには図の下のボタンをクリックしてください。読み込みが始まらない時は図をクリックしてみてください。
いろんな酵素がDMAPPとIPPを使ってさまざまなイソプレノイド分子をつくっている。これら酵素の多くはイソプレン合成酵素を含め共通の折りたたみ構造を持っていて、この構造は「テルペノイド合成酵素型構造」(terpenoid synthase fold)と呼ばれている。ここに4つの事例を示す。イソプレン合成酵素はリン酸を分解しイソプレンを放出する。ファルネシル二リン酸合成酵素(farnesyl diphosphate synthase、1fps)は3つのイソプレン単位をつないでさらに長い鎖をつくる。ボルニル二リン酸合成酵素(bornyl diphosphate synthase、1n20)は、この種のより長くなった鎖から環状構造をつくる。タキサジエン合成酵素(taxadiene synthase、PDBエントリー3p5p)はタキソール(taxol)をつくるのにイソプレン単位を使い、より複雑な構造をつくる。図の下にあるボタンをクリックして対話的操作のできる画像に切り替え、これらの構造をより詳しく見てみて欲しい。
理解を深めるためのトピックス
- イソプレノイド分子は、炭素原子がジグザグに連なった鎖に炭素1原子の枝がいくつかついた独特な形状をしている。代表的な例としてファルネシル二リン酸のページを見たり、化合物検索でクロロフィル、レチノール、βカロテンなどの分子を検索してこれら分子の化学的構造を見たりしてみて欲しい。
- これらの酵素の活性部位にはマグネシウムイオンがよく使われている。これらのイオンが何をしているのか分かるだろうか? 構造情報に基づいて説明してみよう。
参考文献
- 2015 Reconciling functions and evolution of isoprene emission in higher plants. New Phytologist 206 578-582
- 2013 Experimental evidence for efficient hydroxyl radical regeneration in isoprene oxidation. Nature Geoscience 6 1023-1026
- 2012 The model of emissions of gases and aerosols from nature version 2.1 (MEGAN2.1): an extended and updated framework for modeling biogenic emissions. Geoscientific Model Development 5 1471-1492
- 3p5p 2011 Taxadiene synthase structure and evolution of modular architecture in terpene biosynthesis. Nature 469 116-120
- 3n0g 2010 Structure of isoprene synthase illuminates the chemical mechanism of teragram atmospheric carbon emission. Journal of Molecular Biology 402 363-373
- 2008 Isoprene emission from plants: why and how. Annals of Botany 101 5-18
- 1p0n 2003 Crystal structure of the type II isopentenyl diphosphate:dimethylallyl diphosphate isomerase from Bacillus subtilis. Journal of Molecular Biology 329 973-982
- 1n20 2002 Bornyl diphosphate synthase: structure and strategy for carbocation manipulation by a terpenoid cyclase. Proceedings of the National Academy of Science USA 99 15375-15380
- 1i9a 2001 Structure genomics of enzymes involved in sterol/isoprenoid biosynthesis. Proceedings of the National Academy of Science USA 98 12896-12901
- 1fps 1994 Crystal structure of recombinant farnesyl diphosphate synthase at 2.6-A resolution. Biochemistry 33 10871-10877
- 1960 Blue Hazes in the atmosphere. Nature 187 641-643
 の生体高分子学習ポータルサイト
の生体高分子学習ポータルサイト 









