194: 人工設計インスリン(Designer Insulins)
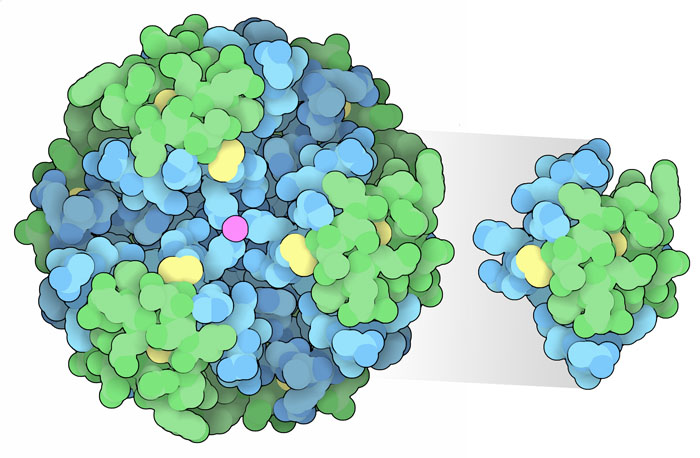
1世紀前には糖尿病(diabetes mellitus)に対する治療法はなく、症状は常に致命的なものであった。ところがこの厳しい現実はインスリン(insulin)の発見により激変した。現在では一転してインスリン治療により糖尿病を制御できるようになり、血糖値上昇による有害な諸症状を最小限に押さえて生き延び、有益な人生を送れる様になった。最初は、ウシやブタなどの家畜から得られたインスリンを使っていて、様々な不純物による問題に悩まされていた。しかし組換えDNAによるバイオテクノロジーを使って、純粋なヒトのインスリンを生産するよう改変を加えた細菌を作り出され、この問題は解消された。これがバイオテクノロジーにおける初期の成功事例となった。ここに示す構造(PDBエントリー1trz)は最初の組換えヒトインスリンを使って解かれた構造で、ヒューマリン(Humulin)という商品名で販売されている。
治療の調整
皮膚の下に組換えヒトインスリンを注射すると、血糖値は急速に低下するが、その効果は数時間のうちに弱まってしまう。この血糖値制御法がよく効くのは食事の直後だけである。体内の各細胞は、食事と食事の間には筋肉や肝臓に蓄えられているグリコーゲン(glycogen)を使ってエネルギーを得ている。通常の環境下であれば、
ゆっくり効くインスリン
ゆっくり効くインスリンを作る方法は、分子構造の知見から着想を得たものである。インスリンは6量体の形で
希望に合った相互作用を作り出す
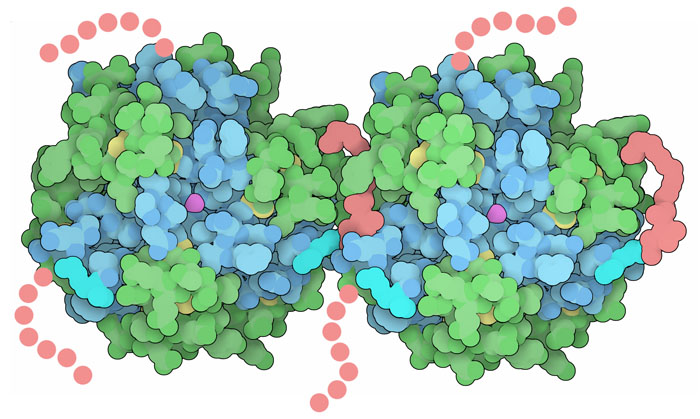
効果が長く持続するインスリンは、分子の末端に長い炭化水素鎖を付加する方法によっても作られてきた。この修飾によって、6量体がいくつか集まり血液中でゆっくり分解される凝集体が作られるようになった。凝集体は血液中にあるタンパク質血清アルブミン(serum albumin)との相互作用もより安定なものにしてくれるので、この人工設計インスリンの効果はさらに持続する。ここに示す構造はデグルデク(Degludec、PDBエントリー4ajx)のものである。1本の炭化水素鎖が2つの6量体の間をつないでいるこの結晶構造から、人工設計インスリンホルモンが皮下に注射された後、どのようにして高次の凝集体を作るのかについてのヒントが得られる。
構造をみる
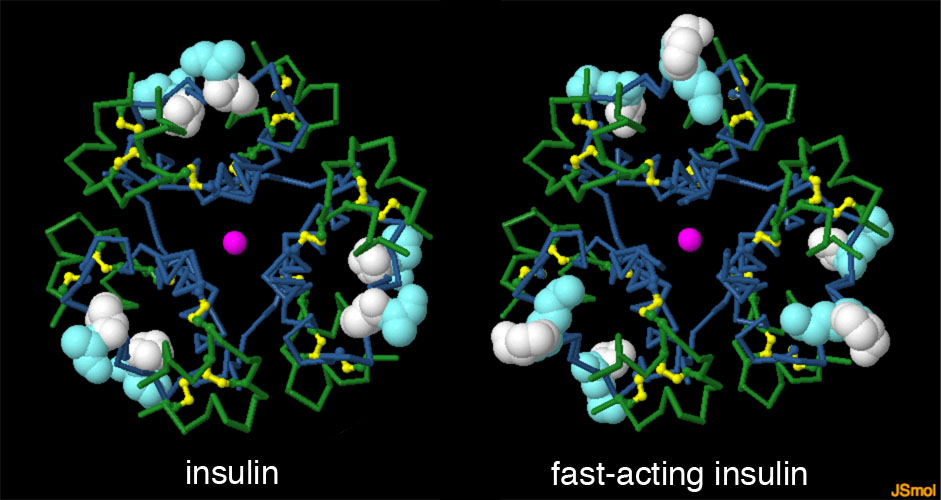
対話的操作のできるページに切り替えるには図の下のボタンをクリックしてください。読み込みが始まらない時は図をクリックしてみてください。
遅効性インスリンは食後すぐに用いる即効性インスリンと組み合わせて使う。6量体を不安定化するという分子的手法を使って作られる即効性インスリンは、血液に入ると速やかに分解されて単量体となる。最初に設計された即効性インスリンは、B鎖のC末端近くにある2つのアミノ酸残基の順番を逆にしただけという最小限の改変を加えただけのものであった。だが、この改変によってインスリン単量体同士の相互作用は弱まり、この変異型6量体は天然のものと比べ200倍も安定性が低いものとなっている。この即効性インスリンはヒューマログ(Humalog、PDBエントリー1lph)という商品名で販売されている。インスリン分子構造の更なる研究によって、電荷のあるアミノ酸を同じ位置に追加しても同じ結果が得られることが分かった。こちらの即効性インスリンはアスパルト(Aspart、PDBエントリー4gbc)という商品名で販売されている。図の下のボタンをクリックして対話的操作のできる画像に切り替え、これらの構造をより詳しく見てみて欲しい。
理解を深めるためのトピックス
- インスリンペーパーモデルの型紙データを使ってペーパーモデルを作ることができます。またインスリンについての解説がPDB-101のサイトにあります。
- 驚くべきことに、フェノール(phenol)やクレゾール(cresol)のような低分子で保存力のある分子はインスリン治療において重要な役割を果たしていて、6量体が血液に到達するまで安定な状態を保ってくれます。PDBに登録されているインスリン構造の多くはこのような分子を含んでいて、6量体を構成する各鎖の間の相互作用を安定なものにしています。
- 鎖1本でも極めて安定なインスリンを設計する方法の探索も行われています。例えば、PDBエントリー2jzqの構造を見てみてください。
参考文献
- 2015 The past, present, and future of basal insulins. Diabetes/Metabolism Research and Reviews DOI:10.1002/dmrr.2763 PMID:26509843
- 2014 The evolution of insulin glargine and its continuing contribution to diabetes care. Drugs 74 911-927 DOI:10.1007/s40265-014-0226-4 PMID:24866023 PMC:PMC4045187
- 4gbc 2013 A T3R3 hexamer of the human insulin variant B28Asp. Biophysical Chemistry 173 1-7 DOI:10.1016/j.bpc.2013.01.003 PMID:23428413
- 4ajx 2012 Ligand-controlled assembly of hexamers, dihexamers, and linear multihexamer structures by the engineered acylated insulin degludec. Biochemistry 52 295-309 DOI:10.1021/bi3008609 PMID:23256685
- 1lph 1995 Role of C-terminal B-chain residues in insulin assembly: the structure of hexameric LysB28ProB29-human insulin. Structure 3 615-622 DOI:10.1016/S0969-2126(01)00195-2 PMID:8590022
- 1trz 1994 Crystallographic evidence for dual coordination around zinc in the T3R3 human insulin hexamer. Biochemistry 33 1512-1517 DOI:10.1021/bi00172a030 PMID:8312271
- 1tyl 1994 The structure of a complex of hexameric insulin and 4'-hydroxyacetanilide. Proceedings of the National Academy of Sciences USA 91 8851-8855 PMID:8090735 PMC:PMC44704
 の生体高分子学習ポータルサイト
の生体高分子学習ポータルサイト 









