189: アミロイド(Amyloids)
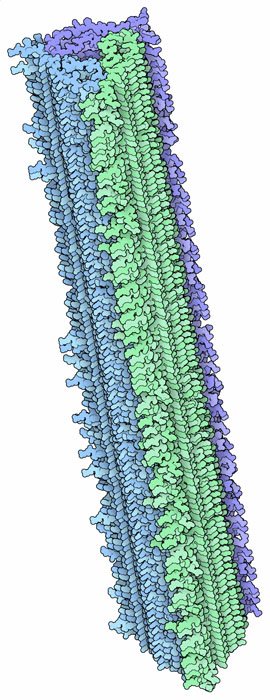
タンパク質は折りたたまれて機能的な形状をとるよう進化してきた。但し、構造の一部にいつもほどけた状態になっている柔軟な綱を必要とするものもある。そして、これらタンパク質は凝集して望まない構造をとることがある。これは危険な結末を招くこととなる。アミロイドβ前駆体タンパク質(amyloid-beta precursor protein)がこれにぴったりの事例と言えるだろう。通常の形状をしている時は、折りたたまれた部分が柔軟な綱でつながれた膜結合タンパク質である。しかし、タンパク質鎖が壊れると、それによってできたペプチドの一部が凝集してアミロイド(amyloid)と呼ばれる長い線維になる。これが細胞の正常な働きを妨げることがある。
クロスβ
この線維は、X線回折を使って解析すると、クロスβパターン(cross-beta pattern)と呼ばれる独特のパターンを示す。この現象は次のようにして起こる。まず線維を構成する小さなペプチドは積み重なって個々のβ鎖を形成する。次に隣り合ったβ鎖との間に水素結合が作られ大きく広がったβシートとなる。この結果、鉄やクモの糸の強さにも匹敵する非常に丈夫な構造ができる。
アミロイドと病気
脳の中にこのような線維ができることは、アルツハイマー病(Alzheimer's disease)の発生につながる。ここに示すアミロイド線維(PDBエントリー2m4j)はアルツハイマー病患者から単離されたもので、どのようにして多数の小さなペプチドが積み重なり、3回対称型の線維を形成するのかを示している。またある種のアミロイド構造は感染性を持つ。狂牛病(mad cow disease)やクールー病(kuru)などのプリオン病(prion diseases)は、アミロイド型タンパク質の摂取が原因となっていることがある。体内に入ったアミロイドはアミロイド線維の鋳型となり、誤った折りたたまれたり凝集してしまったりした体内の通常タンパク質が集まるための核となる。これが更なるアミロイド線維の形成につながる。
アミロイドの研究
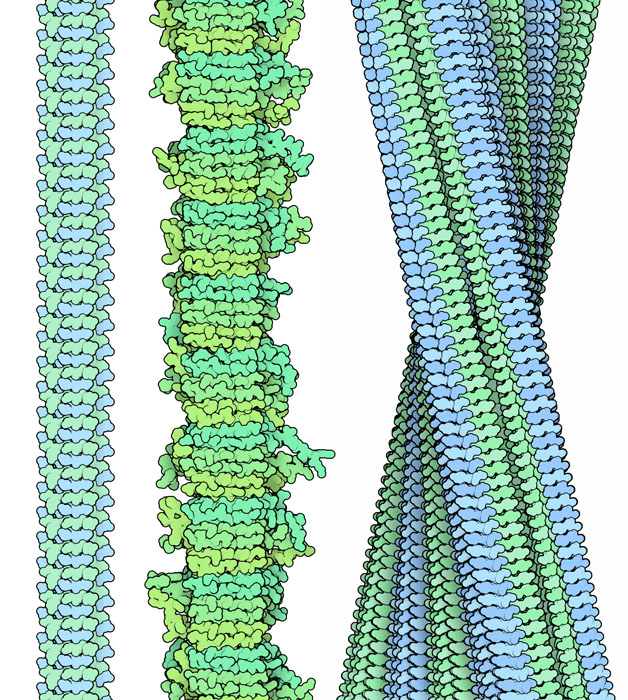
アミロイドの構造は非常に大きく繊維状になっているので、従来型の構造決定手法による解析は困難であった。そこでいくつかの手法が取り入れられた。その1つに、アミロイドタンパク質を切断してより小さな断片とし、結晶化できるようにするというものがある。例えば、左図の左側に示す結晶構造(PDBエントリー3nhc)は、ヒトのプリオンタンパク質から得られた6個のアミノ酸でできたペプチドである。この種の構造から、アミロイドタンパク質が積み重なって広がったβシートを作るのに様々な方法のあることが明らかになった。またいくつかの実験手法を組み合わせたハイブリッド法(hybrid method)が多くの構造決定に用いられてきた。その中には酵母のプリオン(中央、PDBエントリー2kj3)、トランスサイレチン(transthyretin、右、PDBエントリー3zpk)、そして先述のアミロイドβ構造などがある。これらの構造において、局所的な構造的特徴、βシート構造、離れた原子間の接触を決定するのに固体NMR(solid state NMR)が用いられる。一方、線維全体の大きさやサブユニットの数の決定には電子顕微鏡が用いられる。最後に、両方のデータと矛盾しない構造を見出すのに分子設計(モデリング)の手法が使われる。
構造をみる
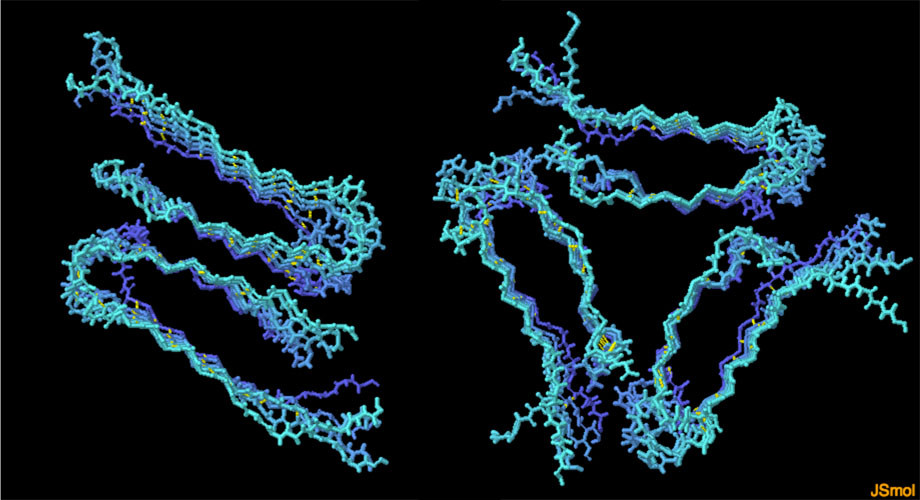
対話的操作のできるページに切り替えるには図の下のボタンをクリックしてください。読み込みが始まらない時は図をクリックしてみてください。
他にもアミロイドの研究を難しくしている要素がある。アミロイドは非常に強い多形性を示し様々な種類の線維を形成することがよくある。ここに2種類のアミロイドβ線維(PDBエントリー2lmn、2lmp)の構造を示す。一方は2回対称性の線維、もう一方は3回対称性の線維を形成したペプチドである。鎖が積み重なって長いβシートとなる時はどちらも非常に似た相互作用をするが、シート間の側面相互作用は両者で異なっている。図の下のボタンをクリックして対話的操作のできる画像に切り替え、これらの構造をより詳しく見てみて欲しい。
理解を深めるためのトピックス
- RCSB PDBのProtein Feature View - アミロイドβ前駆体タンパク質を見ると、線維形成部分がどのようにしてタンパク質の全体の中に組み込まれているのかが分かるでしょう。「Molecular Processing」の「β-a」ラベルを見ると、線維を形成している部分が見つかります。
- アミロイド線維中のβ鎖は様々な様式で関わり合い、並行して隣接するβ鎖が同じ方向を向いているものもあれば、逆方向を向いているものもあります。例えば、PDBエントリー2lmnと2lnqを比較し、表示をリボン表現に設定するとβ鎖の方向が分かるでしょう。
参考文献
- 2015 Amyloid polymorphism: structural basis and neurobiological relevance. Neuron 86 632-645 DOI:10.1016/j.neuron.2015.03.017 PMID:25950632 PMC:PMC4425266
- 3zpk 2013 Atomic structure and hierarchical assembly of a cross-beta amyloid fibril. Proceedings of the National Academy of Science USA 110 5468-5473 DOI:10.1073/pnas.1219476110 PMID:23513222 PMC:PMC3619355
- 2m4j 2013 Molecular structure of beta-amyloid fibrils in Alzheimer's disease brain tissue. Cell 154 1257-1268 DOI:10.1016/j.cell.2013.08.035 PMID:24034249 PMC:PMC3814033
- 2013 Molecular structures of amyloid and prion fibrils: consensus versus controversy. Accounts of Chemical Research 46 1487-1496 DOI:10.1021/ar300282r PMID:23294335 PMC:PMC3632659
- 2012 The amyloid state of proteins in human diseases. Cell 148 1188-1203 DOI:10.1016/j.cell.2012.02.022 PMID:22424229 PMC:PMC3353745
- 3nhc 2010 Crystallographic studies of prion protein (PrP) segments suggest how structural changes encoded by polymorphism at residue 129 modulate susceptibility to human prion disease. Journal of Biological Chemistry 285 29671-29675 DOI:10.1074/jbc.C110.158303 PMID:20685658 PMC:PMC2943325
- 2kj3 2010 Atomic-resolution three-dimensional structure of HET-s(218-289) amyloid fibrils by solid-state NMR spectroscopy. Journal of the American Chemical Society 132 13765-13775 DOI:10.1021/ja104213j PMID:20828131
- 2lmp 2008 Molecular structural basis for polymorphism in Alzheimer's beta-amyloid fibrils. Proceedings of the National Academy of Science USA 105 18349-18354 DOI:10.1073/pnas.0806270105 PMID:19015532 PMC:PMC2587602
- 2lmn 2006 Experimental constraints on quaternary structure in Alzheimer's beta-amyloid fibrils. Biochemistry 45 498-512 DOI:10.1021/bi051952q PMID:16401079 PMC:PMC1435828
 の生体高分子学習ポータルサイト
の生体高分子学習ポータルサイト 









