126: 上皮成長因子(Epidermal Growth Factor)
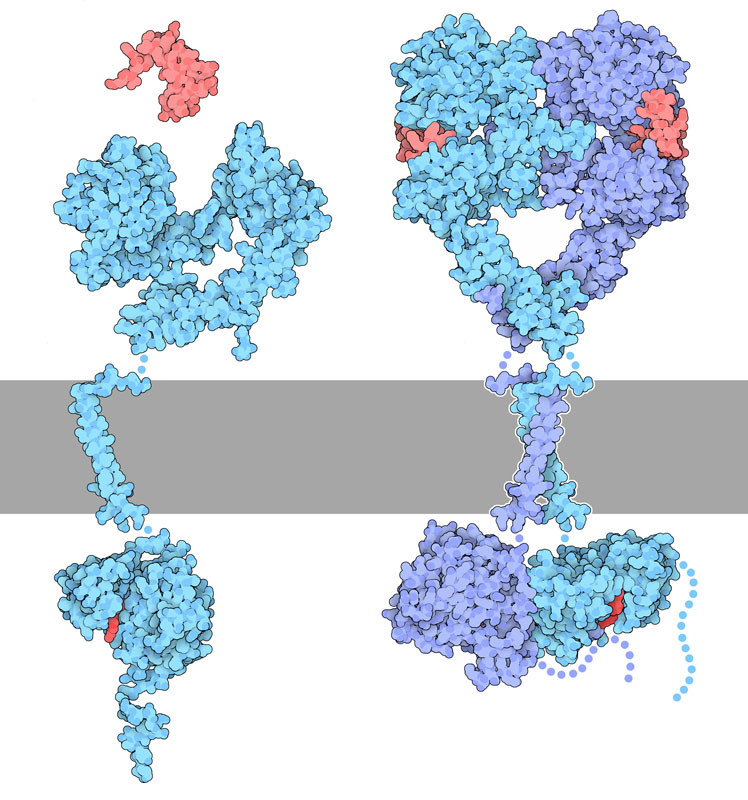
体内にある細胞は常に他の細胞と情報を交換し合い、資源の輸送と利用の調整を行い、そしていつ成長し、いつ休んで、いつ死ぬのかを決定している。このようなメッセージの多くは右図では赤色で示した上皮成長因子(Epidermal Growth Factor、EGF、PDBエントリー 1egf)のような小さなタンパク質が運んでいる。EGFは成長が許可されていることを細胞へ伝えるメッセージなのである。EGFは成長している部位の細胞が放出し、放出した細胞自身または近隣の細胞によって拾われて、拾った細胞の細胞分裂能を活性化させる。細胞表面の受容体がEGFに結合してメッセージを受け取り、細胞内にある信号伝達タンパク質へと中継され、最終的に成長に必要とされる一連の作業が呼び出される。
ドメインと2量体
右図に青色で示した上皮成長因子受容体(epidermal growth factor receptor、EGF受容体)は多くの可動部分を持つ柔軟なタンパク質で、大きな細胞外部分、細胞膜を横切っている部分、キナーゼドメイン(kinase domain、リン酸化酵素ドメイン)、長い柔軟な尾部からできている。細胞の外側(灰色の帯より上)に面した部分は、節でつながった4つのドメインで構成されており、これがEGFを認識する。周辺にEGFがないと、自ら右図左に示すような折りたたんだ構造をとる。そこにEGFが結合すると、受容体は開いてもう1つの同じ受容体と結合し、右図右に示すような2量体を形成する。これによって2つのキナーゼドメイン(図の下方に示した部分)が一緒になる。互いに接近しているため、受容体の長くて柔軟な尾部(ここに示す構造では見えていないので点で示している)にあるチロシン(tyrosine)アミノ酸へリン酸基(phosphate group)を付加することができる。そしてリン酸化された尾部が細胞内にある信号伝達タンパク質を刺激する。
構造的な驚き
EGF受容体は非常に柔軟なので、いくつかの部分に分けて別々に研究されてきた。そのため、この図を作るには複数のPDBファイル(PDBエントリー 1nql、1ivo、2jwa、1m17、2gs6)が必要であった。そしてこの構造にはいくつかの驚くべき点のあることが明らかになった。まず、EGFは上皮成長因子受容体複合体の両側に結合するのが分かった(通常同じような受容体の場合、リガンドは受容体の中央に結合する)。このことから、EGFは受容体に2量体化に適した形状をとらせているのであって、2つの鎖をくっつける働きをしているのではないと思われる。また、キナーゼドメインを注意深く観察することにより、上下非対称な形状が活性化に関与しているのであって、細胞外部分の対称的形状によって活性化されているのではないことも明らかになった。
大きなファミリー
EGFとその受容体は、協同して細胞を成長と発生を制御するという観点でくくられる大きなタンパク質ファミリーに属している。このファミリーには少なくとも7種の類似タンパク質メッセージがあり、例えば、変形増殖因子α(transforming growth factor alpha)、アンフィレギュリン(amphiregulin)、そして4つの受容体が集まって働くErbBまたはHER受容体と呼ばれるものが挙げられる。これらメッセージおよび受容体は、同種あるいは異種の受容体2つをくっつけるまた別のメッセージと混ざっても混乱することなく機能する。こうして、この仕組みによって様々なメッセージを運び、各種細胞の必要に応じた調整を行うことができる。
受容体をOFFにする
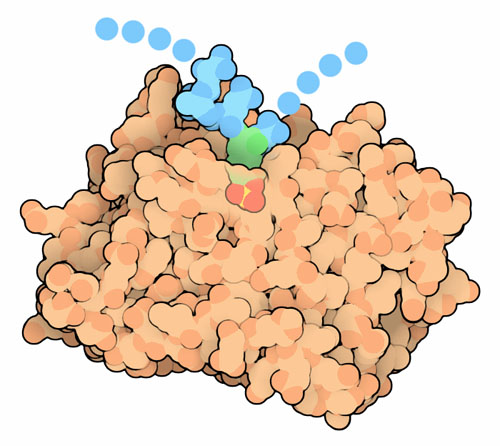
もちろん、信号が上皮成長因子受容体を通して送り終わると、最終的にはOFFにする必要がある。この仕事は、複数に分かれた酵素により行われ、活性化された時に柔軟な尾部へ付加されたリン酸が再び切断される。ここに示したのは、タンパク質チロシンリン酸化酵素1B(protein tyrosine phosphatase 1B、PDBエントリー 1ptu、橙色の部分)およびその活性部位に結合しているリン酸化されたタンパク質鎖の小さな断片である。リン酸化されたチロシンは活性部位の奥深くに埋まっている。
構造を見る
対話的操作のできるページに切り替えるには図の下のボタンをクリックしてください。読み込みが始まらない時は図をクリックしてみてください。
EGFが運ぶ信号は、適切に使わなければ危険を伴う。がんのタイプとしてよくあるのは、EGF信号を止まらなくして通常のEGFによる制御を回避し、自由に成長できるようにしてしまうというものである。この理由から、EGF信号を阻害する薬剤ががんの治療に効果的となる。ここでは2つの事例を挙げる。上図左は、ラパチニブ(lapatinib)という抗がん剤が受容体のキナーゼドメインに結合して、細胞内への信号伝達を阻害しているもの(PDBエントリー 1xkk)である。この薬剤は受容体が使うATPと非常によく似ていて、受容体の活性部位と強固に結合して、本来結合するATPが結合するのを阻害する。また治療抗体(therapeutic antibody)もがんの治療に用いられる。上図右は、HER2/ErbB2の細胞外ドメインにトラスツズマブ(Trastuzumab、商品名はハーセプチン Herceptin)が結合したもの(PDBエントリー 1n8z)と、セツキシマブ(cetuximab)がEGF受容体に結合したもの(PDBエントリー 1yy9)である。構造を詳細に見るには、図の下のボタンをクリックして、対話的操作のできる表示に切り替えてみて欲しい。
理解を深めるためのトピックス
- EGF受容体とヒト成長ホルモン受容体、それぞれが2量体になる方法を比較してみてください。
- EGF受容体およびその類似受容体は、現在がん治療の薬剤開発の対象となっています。薬剤を伴っている他の構造例をPDBで見つけることができますか?
参考文献
- 2009 Ligand-induced ErbB receptor dimerization. Experimental Cell Research 315 638-648
- 2009 The ErbB kinase domain: structural perspectives into kinase activation and inhibition. Experimental Cell Research 315 649-658
- 2008 Structure-based view of epidermal growth factor receptor regulation. Annual Review of Biophysics 37 353-373
 の生体高分子学習ポータルサイト
の生体高分子学習ポータルサイト 









