111: ヒドロゲナーゼ(Hydrogenase)
水素(hydrogen)ガスは普通ではない物質である。通常、水素ガスは安定で化学反応を起こすには強力な触媒を必要とする。ところが、酸素と混合すると、小さな火花があっただけで爆発的な連鎖反応が始まる。水素ガスは最も環境にやさしいエネルギー源として大いに期待できる。他の燃料よりも重量当たりのエネルギー量が大きく、反応に必要なものはエネルギーと純水だけである、といった多くの有利な点がある。一方、重大な欠点がある。貯蔵するには危険で、反応を爆発的ではない制御された方法で行うのが難しいのである。現在のところ、水素で走る車に使うために開発されている燃料電池(fuel cell)は、反応を行う触媒として高価な白金(プラチナ、platinum)を使っている。研究者たちは天然のものから代替となるものを探している。
水素の分割
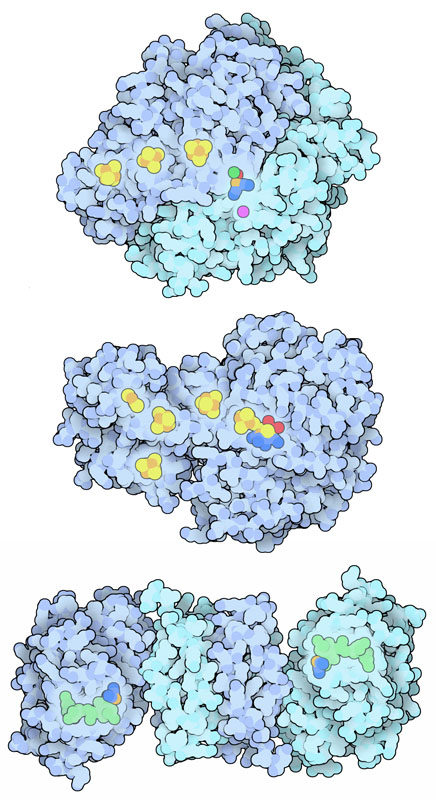
水素ガスを分割する酵素が地球の生命史上で少なくとも3回独立に発達してきた。これらの酵素は、エネルギーとして利用するために水素ガスを分割したり、反応産物としての水素ガスを作り出したりするのに利用される。ここでは3つの例を示す。右図上はニッケル-鉄ヒドロゲナーゼ(nickel-iron hydrogenase、PDBエントリー 2frv)、中央は鉄-鉄ヒドロゲナーゼ(iron-iron hydrogenase、PDBエントリー 1feh)、下は鉄ヒドロゲナーゼ(iron hydrogenase、PDBエントリー 3dagと3f47)である。名前が示すように、いずれも金属イオンを反応に用いる。
水素の制御
3種類のヒドロゲナーゼが異なる組み合わせの金属イオンと補因子(cofactor)を利用して水素(hydrogen)を活性化している。ニッケル-鉄ヒドロゲナーゼと鉄-鉄ヒドロゲナーゼの活性部位はタンパク質の奥深くに埋まっている。反応は小さなチャネルを通って水素が活性部位へと拡散した時に始まる。まず酵素は水素分子を水素イオン(proton、H+)と水素化物(hydride、H-)の2つに分割する。次に、電子が水素化物から引きはがされて電子輸送体の系を伝わって行き、残った2つの水素イオンは同時に表面へと輸送される。鉄ヒドロゲナーゼは少しやり方が違う。活性部位にある特別な補因子が各反応を開始し、この補因子が水素分子が分割された時にできる水素化物を受け取る。
珍しい金属複合体
活性部位複合体は金属イオンとシアン化物(cyanide)や一酸化炭素(carbon monoxide)のような変わった分子との珍しい組み合わせによってできており、システイン(cysteine)アミノ酸によって然るべき場所に保持されている。これらの複雑な活性部位は、熱心な一組の成熟化酵素によって作られる。例えば、ニッケル-鉄ヒドロゲナーゼは活性部位を構築するのに、GTPやATPのエネルギーを使う酵素を少なくとも7つ必要とする。そのような酵素の一つはシャペロンとして働き、活性部位にある重要なシステインに結合してタンパク質をねじり、他の酵素が接触できるようにタンパク質を開く。そして金属イオンを取り込み、リガンドのシアン化物と一酸化炭素を加える。最後に、シャペロンタンパク質がシステインを解放し、成熟したヒドロゲナーゼは新たな活性部位の周辺をぴしっと閉じる。
電子輸送体
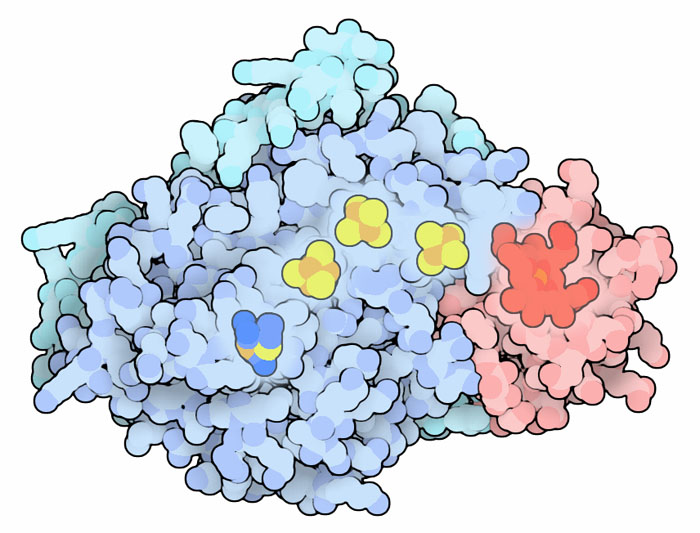
ヒドロゲナーゼが水素から取り出した電子は全て放出先を必要とする。場合によっては、これらの電子はシトクロムなどの電子輸送タンパク質へと運搬される。ここに示した構造(PDBエントリー 1e08)はNMR分光法(NMR spectroscopy)によって解かれたもので、鉄-鉄ヒドロゲナーゼ(青)の持つ電子をシトクロム(ピンク)に運搬しているところをとらえたものである。この複合体に関してより詳細に見るにはプロテオペディアのページを見て欲しい。
構造をみる
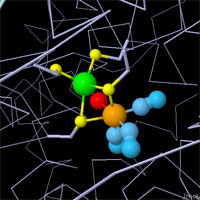
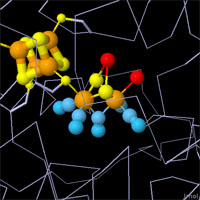
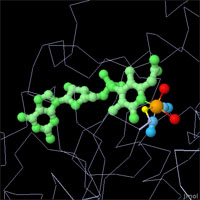
対話的操作のできるページに切り替えるには図の下のボタンをクリックしてください。読み込みが始まらない時は図をクリックしてみてください。
X線結晶解析(X-ray crystallography)によってこれら3種類全ての活性部位が明らかとなったが、まだ謎は残っている。水素は小さすぎて、多くの結晶解析実験では見ることができないため、反応の詳細を見るには他の方法を用いなければならない。活性部位はどれも違っているが、構造はどれも似ていると言わざるを得ない。どの活性部位も分子の中央付近にあり、シアン化物や一酸化炭素といった普通ではないリガンドが鉄原子の周りに存在している。それぞれ別の金属イオンまたは補因子を使って、酸化還元反応を行う鉄原子を助けている。そして3種類ともシステインアミノ酸を使って適切な場所に活性部位を保持する。
理解を深めるためのトピックス
- PDBエントリー1hfeはここで示したのとは別の生物から得られた鉄-鉄ヒドロゲナーゼの構造です。活性部位の鉄原子の周りには違った組み合わせのリガンドがあります。ここに示したもの(PDB:1feh)とPDB:1hfeとの間の類似点と相違点が分かりますか?
- ヒドロゲナーゼを利用して水素の生産と利用を行う技術が確立できるかの研究が行われています。どういう問題に直面していると思いますか?
参考文献
当記事を作成するに当たって参照した文献を以下に示します。
- 2007 Activation and inactivation of hydrogenase function and the catalytic cycle: spectroelectrochemical studies. Chemical Reviews 107 4304-4330
- 2007 Investigating and exploiting the electrocatalytic properties of hydrogenases. Chemical Reviews, 107 4366-4413
- 2007 Metallocenter assembly of the hydrogenase enzymes. Current Opinion in Chemical Biology 11 159-165
 の生体高分子学習ポータルサイト
の生体高分子学習ポータルサイト 









